题目内容
【题目】白云岩矿(含CaO、MgO)常用于生产K2SO4肥及氮钾复合肥。

(1)将白云岩矿石粉碎的目的___________________________;
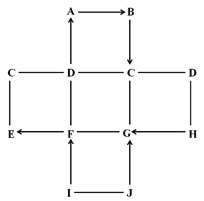
(2)操作a是_______,用到的玻璃仪器除玻璃棒还有_______,玻璃棒作用________;
(3)反应②化学方程式为CaSO4·2H2O + 2 NH4HCO3 == CaCO3↓ + (NH4)2SO4 + CO2↑+ 3H2O,该反应温度需控制在60℃左右,原因________________________;
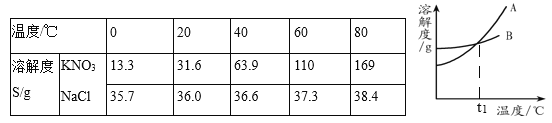
(4)K2SO4在水中溶解度小于(NH4)2SO4,写出反应③的化学方程式________,操作b的步骤:________、冷却结晶、过滤而得到氮钾复合肥。
【答案】 增大接触面积,使反应充分进行(加快反应速率) 过滤 烧杯、漏斗 引流 加快该反应速率且防止碳酸氢铵受热分解 (NH4)2SO4 + 2KCl === K2SO4 ↓+ 2NH4Cl 加热浓缩
【解析】(1)将白云岩矿石粉碎的目的是增大接触面积,使反应充分进行。(2)通过过滤可将固体与液体进行分离,过滤操作用到的玻璃仪器有烧杯、漏斗 ,玻璃棒。其中玻璃棒的作用是引流。(3)碳酸氢铵受热易分解,温度越高反应速率越快。(4)反应③的化学方程式为:(NH4)2SO4 + 2KCl === K2SO4 ↓+ 2NH4Cl ,从溶液中分离出溶质的操作步骤是加热浓缩、冷却结晶、过滤。

练习册系列答案
相关题目