题目内容
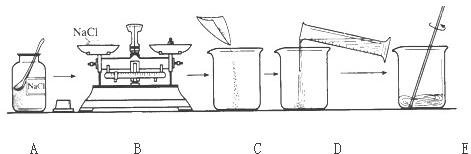
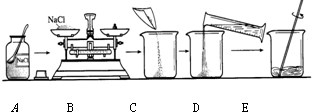
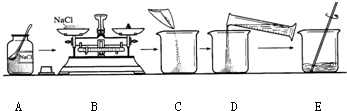
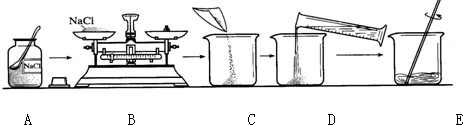
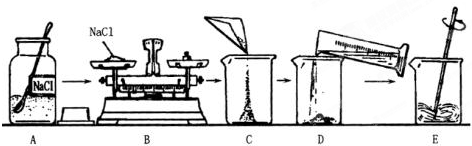
如图是配制50g质量分数为5%的氯化钠溶液的操作过程示意图: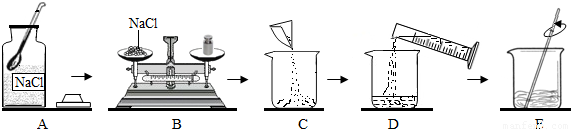
试回答:
(1)B操作中应称量氯化钠的质量是 g.放好砝码和游码后,向托盘上加氯化钠时,若指针偏向分度盘的左边,应进行的操作是 .
(2)D操作应选用 mL的量筒(从10mL、100mL中选择);量水时,量筒必须平放,视线要跟量筒凹液面的 处保持水平.
(3)E操作的作用是 .
【答案】分析:(1)配制50g质量分数为5%的氯化钠溶液,根据溶质质量分数公式可计算出所需氯化钠的质量和水的体积,需要氯化钠的质量为50g×5%=2.5g,水的体积为47.5mL.称量氯化钠时指针偏向分度盘的左边,说明药品多了,应适当减少.
(2)根据量取的液体体积选择适当的量筒;
(3)玻璃棒搅拌的作用是加速溶解.
解答:解:(1)B操作为称取固体氯化钠的质量,根据公式可计算需要氯化钠的质量为50g×5%=2.5g,称量时氯化钠放在左盘,指针偏向分度盘的左边说明氯化钠加多了,应适量减少药品的量;
(2)经计算所需水的体积为47.5mL,所以应该选择100mL量筒来量取,使用量筒读数时,要平视液体凹液面的最低处;
(3)E操作为溶解,使用玻璃棒的作用可以加快食盐的溶解;
故答案为:(1)2.5,减少适量药品至天平衡;(2)100,最低;(3)加速氯化钠溶解.
点评:本题考查了溶液的配制,完成此类题目,可以依据课本已有知识进行回答,所以要求同学们在平时的学习中要加强知识的储备,能够灵活的应用.
(2)根据量取的液体体积选择适当的量筒;
(3)玻璃棒搅拌的作用是加速溶解.
解答:解:(1)B操作为称取固体氯化钠的质量,根据公式可计算需要氯化钠的质量为50g×5%=2.5g,称量时氯化钠放在左盘,指针偏向分度盘的左边说明氯化钠加多了,应适量减少药品的量;
(2)经计算所需水的体积为47.5mL,所以应该选择100mL量筒来量取,使用量筒读数时,要平视液体凹液面的最低处;
(3)E操作为溶解,使用玻璃棒的作用可以加快食盐的溶解;
故答案为:(1)2.5,减少适量药品至天平衡;(2)100,最低;(3)加速氯化钠溶解.
点评:本题考查了溶液的配制,完成此类题目,可以依据课本已有知识进行回答,所以要求同学们在平时的学习中要加强知识的储备,能够灵活的应用.

练习册系列答案
相关题目