题目内容
【题目】铝、铁、铜是我们生活中常见的金属,钛因具有优良的性能,被誉为“未来金属”.
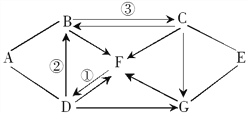
(1)根据图,总结金属具有的物理性质有______.

(2)铝制品具有很好的抗腐蚀性能,原因是______(用化学方程式表示).
(3)铁可形成化合价为+2和+3的两种氧化物,它们的化学式分别为______、______;把铁锈投入稀盐酸中,则预测可观察到的现象是______.
(4)金属钛抗腐蚀性能好,露置于空气中数年,仍光亮如初.以金红石(主要成分是TiO2)为原料生产金属钛的步骤主要有:Ⅰ.在高温下,向金红石与焦炭的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;Ⅱ.在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2.请回答下列问题:
①请写出Ⅱ中的反应方程式:______;
②根据所给信息,下列有关说法不正确的是______.
A.Ⅰ中的方程式是TiO2+C+2Cl2![]() TiCl4+CO2
TiCl4+CO2
B.Ⅱ中的稀有气体的作用是隔绝空气
C.Ⅱ中发生的反应为置换反应
D.金属钛在常温下不易与O2反应
【答案】 导热性、导电性、延展性 4Al+3O2=2Al2O3 FeO Fe2O3 溶液由无色变为黄色 TiCl4+2Mg![]() Ti+2MgCl2 A
Ti+2MgCl2 A
【解析】(1).金属具有的物理性质有有良好的导热性、导电性、延展性,熔点、沸点较高,硬度较大,密度大,通常有金属光泽。(2)铝制品具有很好的抗腐蚀性能,原因是铝和氧气在常温下反应生成致密的氧化铝薄膜,反应方程式为4Al+3O2=2Al2O3(3)化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉约减,得化学式右下角的数字,数字为1时不写;铁可形成化合价为+2和+3的两种氧化物,它们的化学式分别为FeO 、Fe2O3 把铁锈投入稀盐酸中, 铁锈的主要成分氧化铁和盐酸反应生成氯化铁和水;氯化铁溶液为黄色,反应现象是溶液由无色变为黄色;(4)①在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2.反应方程式:TiCl4+2Mg![]() Ti+2MgCl2;②在高温下,向金红石与焦炭的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;反应生成物不可能是二氧化碳;镁和钛的化学性质比较活泼,为防止两金属接触氧气被氧化,反应Ⅱ中的稀有气体的作用是隔绝空气;C.一种单质和一种化合物生成另一种单质和另一种化合物的反应叫置换反应;D.金属钛在常温下不易与O2反应,金属钛抗腐蚀性能好,露置于空气中数年,仍光亮如初.
Ti+2MgCl2;②在高温下,向金红石与焦炭的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;反应生成物不可能是二氧化碳;镁和钛的化学性质比较活泼,为防止两金属接触氧气被氧化,反应Ⅱ中的稀有气体的作用是隔绝空气;C.一种单质和一种化合物生成另一种单质和另一种化合物的反应叫置换反应;D.金属钛在常温下不易与O2反应,金属钛抗腐蚀性能好,露置于空气中数年,仍光亮如初.

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动。
【实验】将一定量稀H2SO4加入到盛有NaOH溶液的烧杯中。
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:除水外,反应后溶液中含有哪些物质?
【假设猜想】针对疑问大家提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4 和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。不合理的是猜想______。
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴酚酞溶液,无明显变化,溶液中一定没有______。
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、氯化钡溶液、碳酸钠溶液,进行如下三个方案的探究。
实验方案 | 方案一:测溶液pH | 方案二:滴加碳酸钠溶液 | 方案三:向溶液中加入铜片 |
实验操作 |
|
|
|
实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 无气泡冒出 |
实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中只有Na2SO4 |
【实验结论】写出方案二中反应的化学方程式_________________________。
通过探究,全班同学一致确定猜想 ______是正确的。
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定。同时指出上面表格中存在两处明显错误,请大家反思。同学们经过反思发现了这两处错误:
(1)实验操作中的错误是_______________________。(说出其中一个即可)
(2)实验中若用氯化钡溶液来进行现象分析,能否得出确切的结论?___为什么?___