��Ŀ����
����Ŀ��ͨ����ѧѧϰ�������Ѿ�������ʵ������ȡ�����һ����ɣ�������ʵ�����ṩ��һЩʵ��װ�ã� 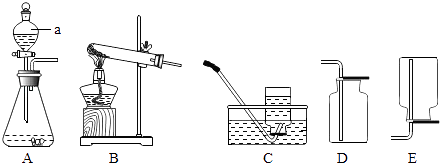
����ͼ���ṩ�������ش����⣮
��1��д��ͼ�б��a���������� ��
��2��ʵ���ҿ��ø�����ء�˫��ˮ���Ʊ�������Ӧѡ�õ�ʵ��װ�ö�ӦΪ �� ������Ӧ�Ļ�ѧ����ʽ�ֱ����� �� ������ѡ�õ�װ������һ�������Ľ����Ľ��ķ����� ��
��3��ͨ���������ϵ�֪���ٰ�����NH3����һ���ܶȱȿ���С�Ҽ�������ˮ�����壬��ˮ��Һ��Ϊ��ˮ���ڰ����ڼ�����������������ͭ��Ӧ����ͭ��ˮ�Ϳ����к����������壮 �����ü����Ȼ�狀��������ƵĹ���������ȡ��������Ӧѡ��ķ�Ӧ����װ�ú��ռ�װ�ö�ӦΪ ��
����д������������ͭ�ڼ��������·�Ӧ�Ļ�ѧ����ʽ�� ��
���𰸡�
��1����Һ©��
��2��B��A��2KMnO4 ![]() K2MnO4+MnO2+O2����2H2O2
K2MnO4+MnO2+O2����2H2O2 ![]() 2H2O+O2�����Թܿ�Ҫ��һ����
2H2O+O2�����Թܿ�Ҫ��һ����
��3��B E��2NH3+3CuO ![]() 3Cu+3H2O+N2
3Cu+3H2O+N2
���������⣺��1������ʵ���ҳ���������֪��a��Һ©������2��ʵ���ҿ��ø�����ؼ��������������ڹ̹̼����ͣ�ѡB��ʵ������Aװ����ȡ����ʱ���Է�Ӧ��ͷ�Ӧ������Ҫ���ǣ���Ӧ���ǹ����Һ�壬����Ҫ���ȣ�������Լ��ǹ���������Һ������������ȷֽ���������غͶ������̺�����������ʽ��2KMnO4 ![]() K2MnO4+MnO2+O2������Ӧ�Ļ�ѧ����ʽ2H2O2
K2MnO4+MnO2+O2������Ӧ�Ļ�ѧ����ʽ2H2O2 ![]() 2H2O+O2����Ϊ��ֹ������ط�ĩ���뵼�ܣ�����ø��������ȡ����ʱ���Թܿ�Ҫ��һ��������3���ٷ�Ӧ���״̬�ǹ�̬����Ӧ�����Ǽ��ȣ�Ӧѡ�̩��̼����͵ķ���װ�ã��������ܶȱȿ���С����������ˮ���������ſ������ռ������Դ��ǣ�B E �ڿ����к������������ǵ���������������ͭ��������ͭ��ˮ�͵��������Դ��ǣ�2NH3+3CuO
2H2O+O2����Ϊ��ֹ������ط�ĩ���뵼�ܣ�����ø��������ȡ����ʱ���Թܿ�Ҫ��һ��������3���ٷ�Ӧ���״̬�ǹ�̬����Ӧ�����Ǽ��ȣ�Ӧѡ�̩��̼����͵ķ���װ�ã��������ܶȱȿ���С����������ˮ���������ſ������ռ������Դ��ǣ�B E �ڿ����к������������ǵ���������������ͭ��������ͭ��ˮ�͵��������Դ��ǣ�2NH3+3CuO ![]() 3Cu+3H2O+N2
3Cu+3H2O+N2
�𰸣���1����Һ©����2��B��A 2KMnO4 ![]() K2MnO4+MnO2+O2����2H2O2
K2MnO4+MnO2+O2����2H2O2 ![]() 2H2O+O2���� �Թܿ�Ҫ��һ��������3����B E ��2NH3+3CuO
2H2O+O2���� �Թܿ�Ҫ��һ��������3����B E ��2NH3+3CuO ![]() 3Cu+3H2O+N2
3Cu+3H2O+N2
�����㾫����������Ĺؼ�����������������ȡװ�õ����֪ʶ�����շ���װ�ã��̹̼����͡���Һ�������ͣ��Լ����������ռ����������⣬�˽��ռ�װ�ã��������ʵ��ܶȡ��ܽ��ԣ���ˮ���ռ�ʱ�������ݾ�������ð��ʱ���ռ����տ�ʼ�ų������Թ��еĿ����������ſ������ռ�����ʱ�������쵽����ƿ�ײ���

 ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�