题目内容
【题目】下列图像能正确反映其对应操作中某物质质量变化关系的是( )
A.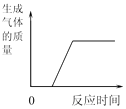 将生锈铁钉放入过量的稀盐酸
将生锈铁钉放入过量的稀盐酸
B.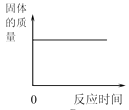 将一定质量的红磷放在盛有氧气的密闭容器中燃烧
将一定质量的红磷放在盛有氧气的密闭容器中燃烧
C.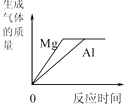 将等质量的镁和铝分别放入足量的稀硫酸中
将等质量的镁和铝分别放入足量的稀硫酸中
D.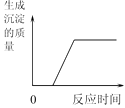 向氢氧化钠和氯化钡的混合溶液中滴加过量的稀硫酸
向氢氧化钠和氯化钡的混合溶液中滴加过量的稀硫酸
【答案】A
【解析】A、将生锈的铁钉放入过量的稀盐酸中,先是外层的铁锈(氧化铁)与盐酸反应,生成氯化铁和水,故开始无气体产生;接着是铁与盐酸反应,生成氯化亚铁和氢气,且随反应的进行,气体的量不断增大,直至铁完全反应不再改变,正确,A符合题意;
B、将一定质量的红磷放在盛有氧气的密闭容器中燃烧,根据质量守恒定律可知,生成的五氧化二磷的质量=磷的质量+氧气的质量,故固体的质量会增加,错误,B不符合题意;
C、将等质量的镁和铝分别放入足量的稀硫酸中,由于镁比铝活泼,故镁生成氢气的速度快,即在相同时间内,镁反应所放出氢气的质量大于铝,也就是表示镁的斜线要更靠近纵轴;但由于酸是足量的,故镁、铝均完全反应,根据金属与足量的酸反应,放出氢气的质量= ![]() ,可知等质量的镁和铝与足量稀硫酸反应时,所放出氢气的质量大小取决于两金属的化合价与相对原子质量的比,可假设两种金属的相同质量为m,则它们与足量稀硫酸完全反应放出氢气的质量分别为:镁完全反应产生氢气的质量=
,可知等质量的镁和铝与足量稀硫酸反应时,所放出氢气的质量大小取决于两金属的化合价与相对原子质量的比,可假设两种金属的相同质量为m,则它们与足量稀硫酸完全反应放出氢气的质量分别为:镁完全反应产生氢气的质量= ![]() ×m=
×m= ![]() ;铝完全反应产生氢气的质量=
;铝完全反应产生氢气的质量= ![]() ×m=
×m= ![]() 。因为
。因为 ![]() <
< ![]() ,所以等质量的镁与足量硫酸完全反应,所产生的氢气质量要小于铝,错误,C不符合题意;
,所以等质量的镁与足量硫酸完全反应,所产生的氢气质量要小于铝,错误,C不符合题意;
D、向氢氧化钠和氯化钡的混合溶液中滴加过量的稀硫酸,由于氯化钡与稀硫酸反应,生成了不溶于酸的硫酸钡沉淀,故反应开始就会有硫酸钡沉淀生成,错误,D不符合题意;
所以答案是:A.
【考点精析】本题主要考查了金属材料的选择依据和质量守恒定律及其应用的相关知识点,需要掌握黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属;①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏才能正确解答此题.
