题目内容
实验室欲抽取88克CO2用于实验研究,则需要多少克CaCO3与足量的稀盐酸反应才可以制取得到?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据制取88gCO2的质量,由反应的化学方程式计算出需要碳酸钙的质量即可.
解答:设需要碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 88g
=
x=200g
答:需要碳酸钙的质量为200g.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 88g
| 100 |
| x |
| 44 |
| 88g |
x=200g
答:需要碳酸钙的质量为200g.
点评:本题难度不大,掌握有关化学式与化学方程式的计算是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
用10mL规格的量筒量取7.5mL的液体,量取的过程中俯视读数,则所取液体的实际体积( )
| A、大于7.5mL |
| B、等于7.5mL |
| C、小于7.5mL |
| D、无法确定 |
钠原子和钠离子的结构示意图如图,其中说法错误的是( )


| A、钠原子有3个电子层,钠离子有2个电子层 |
| B、钠原子和钠离子的质子数都是11 |
| C、1个钠原子在化学反应中可失去1个电子形成钠离子 |
| D、钠原子和钠离子的性质相同 |
下列粒子中属于阴离子的是( )
A、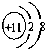 |
B、 |
C、 |
D、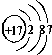 |
 钢铁是人们日常生活中不可缺少的材料,厨具、建筑物中都大量使用了金属材料.
钢铁是人们日常生活中不可缺少的材料,厨具、建筑物中都大量使用了金属材料.