题目内容
【题目】按要求回答问题:
①空气中含有氮气、氧气、稀有气体、二氧化碳等,其中含量最多的气体是______,造成“温室效应”的气体是_________(均用化学式表示)。
②“沙里淘金”说明黄金在自然界以_______(填“游离态”或“化合态”)形式存在。
③水是一种重要的自然资源。
I.生产自来水的过程中不能加入或通入的物质是____(选填编号)。
A.明矾 B.活性炭 C.氯气 D.硫酸铜
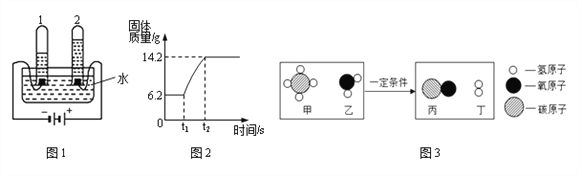
II.下图1电解水实验揭示了水的组成。其中得到氧气的试管是_____(填“1”或“2”);检验试管中氧气的方法是_________________。
④氧气是一种化学性质比较活泼的气体,氧气中点燃红磷的实验过程,固体质量的变化如下图2所示。
I.从燃烧条件分析,固体质量在t1前没有发生变化的原因是_________________。
II.该反应的化学方程式为_________________。
III.参加反应的氧气质量为_________g。
⑤甲烷是天然气的主要成分,能和水反应制水煤气(混合气体),其反应的微观示意图如下图3所示。四种物质中,可作燃料的是_______(填化学式),该反应中生成物丙和丁的质量比为________。
【答案】N2CO2游离态D2带火星的木条伸入试管中,复燃则是氧气温度未达到红磷的着火点4P+5O2 ![]() 2P2O58.0CH4、 CO 、H214:3
2P2O58.0CH4、 CO 、H214:3
【解析】①空气中各成分的含量按体积分数计算,氮气占78%,氧气占21%,稀有气体占0.94%,二氧化碳占0.03%,空气中含有氮气、氧气、稀有气体、二氧化碳等,其中含量最多的气体是氮气,造成“温室效应”的气体是二氧化碳。②物质以化合物形式存在时称为化合态,以单质存在时称为游离态,“沙里淘金”说明黄金在自然界以游离态存在,硫酸铜是重金属盐,能使蛋白质变性,使人中毒。生产自来水的过程中不能加入硫酸铜。II、电解水时正极生成的是氧气,负极生成的是氢气,氢气是氧气体积的2倍;得到氧气的是试管2,检验试管中氧气的方法是将带火星的木条靠近试管2中的气体,木条复燃,证明是氧气。I.燃烧需要同时具备的三个条件:物质有可燃性、温度达可燃物的着火点、与氧气充分接触;灭火时只需要破坏一个条件即可。从燃烧条件分析,固体质量在t1前没有发生变化的原因是温度未达到红磷的着火点。II.该反应的化学方程式为4P+5O2 ![]() 2P2O5。III.由质量守恒定律可知,参见反应的各物质的质量总和等于反应后生成的各物质的质量总和。所以参加反应的氧气质量为14.2g-6.2g=8g。甲烷有可燃性,可做燃料。甲烷燃烧的方程式为CH4 + H2O 点燃 CO +3H2 ,物质的质量比等于化学计量数和相对分子质量乘积的比,所以该反应中生成物一氧化碳和氢气(的质量比为28:6=14:3。
2P2O5。III.由质量守恒定律可知,参见反应的各物质的质量总和等于反应后生成的各物质的质量总和。所以参加反应的氧气质量为14.2g-6.2g=8g。甲烷有可燃性,可做燃料。甲烷燃烧的方程式为CH4 + H2O 点燃 CO +3H2 ,物质的质量比等于化学计量数和相对分子质量乘积的比,所以该反应中生成物一氧化碳和氢气(的质量比为28:6=14:3。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】在元旦联欢晚会上,化学老师表演了“滴水生火”的魔术。先用棉花将淡黄色的过氧化钠(Na2O2)固体包在其中,然后将少量水滴到棉花上,棉花团剧烈燃烧起来。
同学们感到很惊讶,于是展开探究。
【提出问题】棉花为什么会发生燃烧?
【猜想与假设】
①过氧化钠与水反应生成氢氧化钠、氧气。
②过氧化钠与水反应生成氢氧化钠和________气。
③过氧化钠与水反应放出大量热。
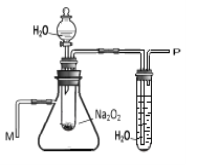
【设计并实验】同学们利用右图所示装置进行了如下探究。
编 号 | 主要实验操作 | 实验现象 | 实验结论 |
打开装置中分液漏斗的活塞,滴加适量水后,关闭活塞。 | |||
将带火星的木条接近P处 | B瓶中有气泡产生;带 火星的木条复燃 | _________ | |
③ | _________ | _________ | 过氧化钠与水反应放 出大量热 |
【解释与结论】
(1)同学们设计实验时,增加了防止发生爆炸的装置B,其原因是_________。
(2)经测定,过氧化钠与水反应还有氢氧化钠生成,该反应的化学方程式为________。
(3)将少量水滴到包有Na2O2固体的棉花上,棉花团剧烈燃烧起来的原因是_________。
