题目内容
【题目】谜语“闻有刺鼻味,含量平均分.酸雨由它造,追捕无影踪.”该物质是( )
A.CO
B.CO2
C.SO2
D.NO2
【答案】C
【解析】解:“闻有刺鼻味,含量平均分.酸雨由它造,追捕无影踪.”中描述的性质、元素质量比符合二氧化硫,因为二氧化硫是一种有刺激性气味的气体,是形成酸雨的重要物质,组成元素中,硫元素和氧元素的质量比是1:1.
故选C.

【题目】根据如图所示实验,回答问题.
|
|
|
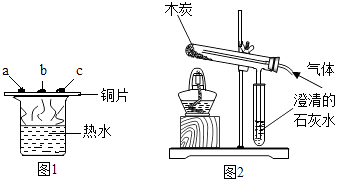
实验1 | 实验2 | 实验3 |
(1)实验1中观察到的现象是 .
(2)实验2中的现象说明二氧化碳具有性质.
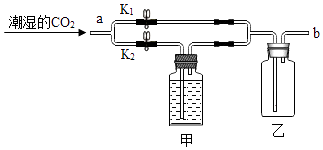
(3)实验3甲瓶中盛放的浓H2SO4具有吸水性,乙瓶中盛放的是用石蕊溶液染成紫色的干燥小花.若证明使石蕊变色的是碳酸而不是二氧化碳的实验操作是 .
【题目】某兴趣小组以“稀硫酸与氢氧化钠溶液能否发生反应”为课题进行了科学探究.如图1所示,小组同学向烧杯中的氢氧化钠溶液加入稀硫酸.一会儿发现忘记了滴加指示剂,因此,他们停止滴加稀硫酸,并对烧杯内稀硫酸与氢氧化钠溶液是否发生了反应进行探究. 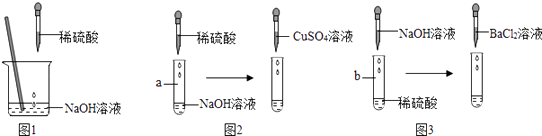
(1)小组同学设计了以下实验方案:
实验步骤 | 实验现象 | 实验结论 |
在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量反应后的溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,读溶液的pH | pH7 | 稀硫酸与氢氧化钠溶液发生了反应,且稀硫酸过量了. |
(2)写出该反应的化学方程式: .
(3)同学们经过讨论一致认为,不用上述方法,用其他试剂也可以证明稀硫酸与氢氧化钠溶液能发生反应.于是分成甲、乙两组继续试验. 甲组实验:探究CuSO4溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应.
【实验操作及现象】如图2,向a试管中滴加足量稀硫酸时无明显现象,再滴加CuSO4溶液时没有出现蓝色沉淀.
【实验结论】通过以上实验操作及现象,你认为用CuSO4溶液(填“可以”或“不可以”)证明稀硫酸与氢氧化钠溶液能发生反应.
乙组实验:探究BaCl2溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应.
【实验操作及现象】如图3,向b试管中滴加足量NaOH溶液时无明显现象,再滴加BaCl2溶液时出现白色沉淀.
【实验结论】通过以上实验操作及现象,你认为用BaCl2溶液(填“可以”或“不可以”)证明稀硫酸与氢氧化钠溶液能发生反应.理由是 .