题目内容
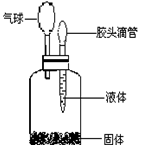
(9分)要除去铜屑中的少量铁屑,某同学设计了以下两个实验方案:
(1)写出两个实验方案中有关反应的化学方程式。
① ▲ , ② ▲ 。
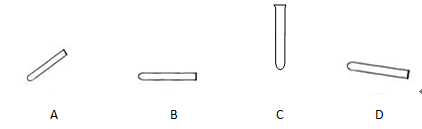
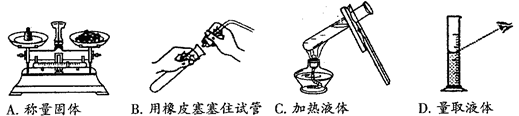
(2)过滤时要用到下列仪器中的 ▲ (填序号)。
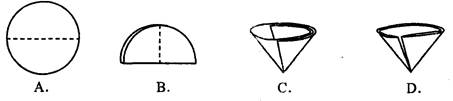
(3)过滤时需要将圆形滤纸折叠处理,下列图示错误的是 ▲ (填序号)。
(4)方案①洗涤的目的是 ▲ 。

(1)写出两个实验方案中有关反应的化学方程式。
① ▲ , ② ▲ 。
(2)过滤时要用到下列仪器中的 ▲ (填序号)。
| A.研钵 | B.烧杯 | C.漏斗 | D.试管 |
(4)方案①洗涤的目的是 ▲ 。

本题考查的是金属的化学性质,过滤的原理、方法及其应用,书写化学方程式。
(1)在金属活动性顺序中,只有氢前的金属才可以和稀酸溶液反应生成氢气,只有前面的金属才可以把排在它后面的金属从盐溶液中置换出来,由于铁既在铜前,也在氢前,所以铁既能和硫酸铜溶液反应也能和稀硫酸反应,从而可以达到除去铁的目的。铁与硫酸铜反应生成铜和硫酸亚铁,铁和稀硫酸反应生成硫酸亚铁和氢气,故化学方程式为:
Fe+CuSO4═Cu+FeSO4;Fe+2H2SO4=FeSO4+H2↑
(2)过滤时要用到铁架台或三角架,漏斗和滤纸,烧杯、玻璃棒等,故选BC;
(3)过滤时要用到漏斗,将滤纸对折再对折,叠成一面有三层滤纸的圆锥形的形状,故选D;
(4)铁与硫酸铜溶液反应生成铜和硫酸亚铁,经过滤后,铜表面会留有硫酸亚铁溶液,故要洗涤除去。
(1)在金属活动性顺序中,只有氢前的金属才可以和稀酸溶液反应生成氢气,只有前面的金属才可以把排在它后面的金属从盐溶液中置换出来,由于铁既在铜前,也在氢前,所以铁既能和硫酸铜溶液反应也能和稀硫酸反应,从而可以达到除去铁的目的。铁与硫酸铜反应生成铜和硫酸亚铁,铁和稀硫酸反应生成硫酸亚铁和氢气,故化学方程式为:
Fe+CuSO4═Cu+FeSO4;Fe+2H2SO4=FeSO4+H2↑
(2)过滤时要用到铁架台或三角架,漏斗和滤纸,烧杯、玻璃棒等,故选BC;
(3)过滤时要用到漏斗,将滤纸对折再对折,叠成一面有三层滤纸的圆锥形的形状,故选D;
(4)铁与硫酸铜溶液反应生成铜和硫酸亚铁,经过滤后,铜表面会留有硫酸亚铁溶液,故要洗涤除去。

练习册系列答案
相关题目