题目内容
【题目】某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数,实验测得相关数据如下图所示:
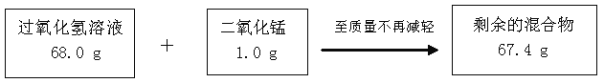
(1)反应生成氧气的质量为 g,其物质的量为 mol。
(2)根据化学方程式计算该过氧化氢溶液中过氧化氢的物质的量。
(3)该过氧化氢溶液中溶质质量分数为 。
【答案】(1)1.6 0.05(2)0.1mol (3)5%。
【解析】
试题分析:根据质量守恒定律知道反应生成氧气的质量为=68.0克+1.0克-67.4克=1.6克g,其物质的量为=1.6/32=0.05摩尔。
设H2O2的物质的量为xmol
2H2O2 MnO2 2H2O+ O2↑
2 1
X 0.05
X=0.1(mol)
设生成1.6克氧气需要过氧化氢的质量为X,
2H2O2 MnO2 2H2O+ O2↑
68 32
X 1.6克
列比利式得:68:X=32:1.6克 解得X=3.4克
该过氧化氢溶液中溶质质量分数为=3.4克/68克*100%=5%。

练习册系列答案
相关题目