题目内容
用红磷在空气中燃烧的实验,可测定氧气约占空气总体积的体积分数,还可间接推测出氮气的一条物理性质,即:________,同时也说明氮气化学性质比氧气的化学性质________,应用此性质推出氮气的一条用途是________.
难溶于水 不活泼(或稳定) 作保护气(或食品包装充气防腐)
分析:只有熟悉用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,才能正确解答本题.
解答:用红磷在空气中燃烧的实验,可测定氧气约占空气总体积的体积分数,还可间接推测出氮气难溶于水的物理性质,同时也说明氮气化学性质比氧气的化学性质不活泼(或稳定),因此氮气可作保护气(或食品包装充气防腐).
故答案为:
难溶于水;不活泼(或稳定);作保护气(或食品包装充气防腐)
点评:本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度稍大.
分析:只有熟悉用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,才能正确解答本题.
解答:用红磷在空气中燃烧的实验,可测定氧气约占空气总体积的体积分数,还可间接推测出氮气难溶于水的物理性质,同时也说明氮气化学性质比氧气的化学性质不活泼(或稳定),因此氮气可作保护气(或食品包装充气防腐).
故答案为:
难溶于水;不活泼(或稳定);作保护气(或食品包装充气防腐)
点评:本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度稍大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
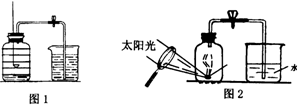



 用来测定空气成分的方法有很多,课本上就是用红磷在空气中燃烧的测定方法.实验过程有:
用来测定空气成分的方法有很多,课本上就是用红磷在空气中燃烧的测定方法.实验过程有: