��Ŀ����
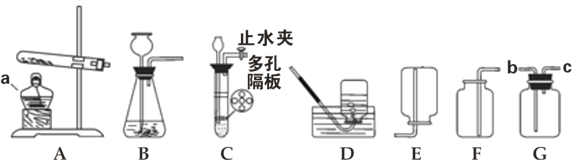
����Ŀ����ͼ��ʾA��G�dz��л�ѧ�г��������ʣ���Ӧ�����Ͳ��ֲ�����ʡ�ԣ���������ʾ��ܷ�Ӧ����������ʾת����ϵ��������A������θҺ�к��е��ᣬB��C�����Ԫ����ͬ��D��һ�ֺ�ɫ��ĩ��F����Է���������С���������ش��������⣮
��1��д������E��һ����;�� ��
��2��A��G���������У��������� �֣�
��3��F��E�ķ�Ӧ������ ��
��4��A��B��Ӧ�Ļ����������ڣ� ��
��5��F��G�Ļ�ѧ����ʽ�ǣ� �� C��D��Ӧ�Ļ�ѧ����ʽ�ǣ� ��
���𰸡���1����������������
��2��4��
��3���ų�������
��4�����ֽⷴӦ��
��5��2H2O![]() 2H2��+O2����Fe2O3+3CO
2H2��+O2����Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
�����������������
��1��A��G�dz��л�ѧ�г��������ʣ�A������θҺ�к��е��ᣬ����A���ᣬF����Է���������С�����������F��ˮ��D��һ�ֺ�ɫ��ĩ�������D�ᷢ����Ӧ������D����������C������������Ӧ��B��C�����ת����B��C�����Ԫ����ͬ������C��һ����̼��B�Ƕ�����̼�����������G��G��ˮ�����ת��������G��������ˮ���ɵ�E������ᷢ����Ӧ������E���������ƣ�������֤���Ƶ���ȷ������E���������ƣ����Ը�������������
��2��ͨ���Ƶ���֪��A�����ᣬB�Ƕ�����̼��C��һ����̼��D����������E���������ƣ�F��ˮ��G������������A��G���������У���������4�֣�
��3��F��E�ķ�Ӧ��ˮ�������Ʒ�Ӧ�����������ƣ�ʵ�������ǣ��ų�������
��4��A��B�ķ�Ӧ�������̼��Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͷ�����̼�����Ի�����Ӧ�������ڸ��ֽⷴӦ��
��5��F��G�ķ�Ӧ��ˮ��ͨ���������������������������ѧ����ʽ�ǣ�2H2O![]() 2H2��+O2����C��D�ķ�Ӧ��һ����̼���������ڸ��µ������·�Ӧ�������Ͷ�����̼����ѧ����ʽ�ǣ�Fe2O3+3CO
2H2��+O2����C��D�ķ�Ӧ��һ����̼���������ڸ��µ������·�Ӧ�������Ͷ�����̼����ѧ����ʽ�ǣ�Fe2O3+3CO![]() 2Fe+3CO2���ʴ�Ϊ����1������������������2��4����3���ų���������4�����ֽⷴӦ����5��2H2O
2Fe+3CO2���ʴ�Ϊ����1������������������2��4����3���ų���������4�����ֽⷴӦ����5��2H2O![]() 2H2��+O2����Fe2O3+3CO
2H2��+O2����Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2

 һ����ʦȨ����ҵ��ϵ�д�
һ����ʦȨ����ҵ��ϵ�д�����Ŀ��ij��Ƭ�ı�ǩ��ͼ����֪�˸�Ƭ�ɷ���ֻ��̼��ƺ��и�Ԫ�ء�
��Ҫ�ɷ֣�̼��ƣ�CaCO3��ά����D |
�� ��ÿƿ50Ƭ������40�� |
�� �� ����ÿƬ����0.75�� |
��1������ά����D2�����ڸƵ����գ����Ļ�ѧʽΪC28H44O��������Է�������Ϊ_______��
��2�����ݱ�ǩ�еĺ������������ÿƬ��Ƭ��̼��Ƶĺ���Ϊ_________g��
��3����ǩ�еĺ������Ƿ����__________����ǡ���?
����Ŀ��ʵ����ϣ�ijС���ͬѧ����ʯ�ҽ��С���ѧ��Ӧ�������ı仯��ʵ��ʱ���֣����״��ʯ���м�������ˮ��û�����Ե��¶ȱ仯��Ϊȷ����ԭ����������ʵ��̽����
��������⡿��ʯ���Ƿ���ʣ���ɷ���ʲô��
���������ϡ����������ܽ�������������¶ȱ仯�������ᷴӦ���������ɡ�
����������衿ͬѧ����Ϊ��ʯ����Ʒ�Ѿ����ʣ�������ɷ�����������4�ֲ��롣
����1�������ƺ��������ƣ�
����2�������ƺ�̼��ƣ�
����3��______��
����4�������ơ��������ƺ�̼��ơ�
������ʵ�顿ͬѧ�ǽ�������Ʒ�������ͼ��ʾ���̽���ʵ�顣
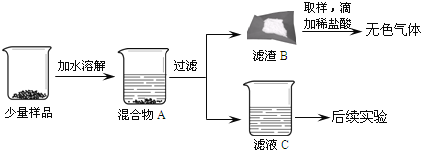
��1�����ܽ���������¶ȼƲ���Һ����¶ȣ������¶ȼ�ʾ�����ߣ�˵����Ʒ��Ӧ�ú���____________�����ۣ�����3��������
��2������B��һ������________���û�ѧ����ʽ��ʾ���ɸ����ʵķ�Ӧ________��
���ۣ��ٿ�״��ʯ�ұ��淢�����ʣ��ڲ���1��������
��3��Ϊ��֤��ҺC�ijɷ֣����к���ʵ�顣
ʵ����� | ʵ������ | ʵ����� |
______ | ______ | ����Һ������Ϊ�������� �ڲ���4����������2������ |
����˼�����ۡ�
�е�ͬѧ��Ϊ����ʵ����̲��ܵó�����4����������2�������Ľ��ۣ�������_________��