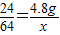题目内容
现提供信息“4.8g镁粉与足量的氧化铜粉末完全反应生成铜和氧化镁”.
(1)请你自己提一个问题,并完成解答.
问题:________;
解答过程:________.
(2)有位同学列出的比例式是:24:64=4.8:a,请推测其中a所表示的内容.a表示:________.
解:(1)设4.8g镁粉与足量的氧化铜粉末完全反应生成铜的质量是x
Mg+CuO Cu+MgO
Cu+MgO
24 64
4.8g x
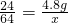
x=12.8g
答:4.8g镁粉与足量的氧化铜粉末完全反应生成铜的质量是4.8g.
(2)由(1)我们可以看出,24和64分别是镁和铜的相对原子质量,4.8是参加反应的镁的质量,故a应是反应生成的铜的质量.
故答案为:
(1)4.8g镁粉与足量的氧化铜粉末完全反应生成铜的质量是多少?;设4.8g镁粉与足量的氧化铜粉末完全反应生成铜的质量是x
Mg+CuO Cu+MgO
Cu+MgO
24 64
4.8g x
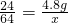
x=12.8g
答:4.8g镁粉与足量的氧化铜粉末完全反应生成铜的质量是4.8g.
(2)反应生成的铜的质量;
分析:(1)可以根据反应物的质量求生成物的质量,根据化学方程式的计算即可求出.
(2)根据24和64分别是镁和铜的相对原子质量,4.8是参加反应的镁的质量,可得a代表的意义.
点评:此题出得非常新颖,既考查了学生根据化学方程式的计算,又考查了学生提出问题解决问题的能力.
Mg+CuO
 Cu+MgO
Cu+MgO24 64
4.8g x
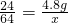
x=12.8g
答:4.8g镁粉与足量的氧化铜粉末完全反应生成铜的质量是4.8g.
(2)由(1)我们可以看出,24和64分别是镁和铜的相对原子质量,4.8是参加反应的镁的质量,故a应是反应生成的铜的质量.
故答案为:
(1)4.8g镁粉与足量的氧化铜粉末完全反应生成铜的质量是多少?;设4.8g镁粉与足量的氧化铜粉末完全反应生成铜的质量是x
Mg+CuO
 Cu+MgO
Cu+MgO24 64
4.8g x
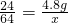
x=12.8g
答:4.8g镁粉与足量的氧化铜粉末完全反应生成铜的质量是4.8g.
(2)反应生成的铜的质量;
分析:(1)可以根据反应物的质量求生成物的质量,根据化学方程式的计算即可求出.
(2)根据24和64分别是镁和铜的相对原子质量,4.8是参加反应的镁的质量,可得a代表的意义.
点评:此题出得非常新颖,既考查了学生根据化学方程式的计算,又考查了学生提出问题解决问题的能力.

练习册系列答案
相关题目