题目内容
人类的生产和生活都离不开金属.Ⅰ.金属元素在自然界中分布很广,在地壳中主要以矿物形式存在.图1中的矿石的主要成分不属于氧化物的是______(填序号).
Ⅱ.铁是应用最广泛的金属.
(1)图2是工业炼铁示意图.其中,焦炭的作用是燃烧提供能量和______;写出有铁生成的化学方程式______ 2Fe+3CO2
【答案】分析:Ⅰ.根据矿石的成分及氧化物的定义分析;
Ⅱ.(1)根据炼铁炉内发生的反应,分析焦炭的作用和写出有铁生成的化学方程式;
(2)①一氧化碳具有还原性,可与氧化铁反应生成黑色的铁和二氧化碳,二氧化碳能与氢氧化钙反应生成了碳酸钙沉淀和水.据此分析回答;
②根据尾气中含有一氧化碳,有毒能污染空气分析;
(3)①根据质量守恒定律分析计算混合物中铁元素与氧元素的质量比;
②根据化学式,由氧元素的质量求出氧化铁的质量,即可求出铁粉的质量,再求出混合物中铁粉的质量分数.
解答:解:Ⅰ、由矿石的成分可知,孔雀石的主要成分是Cu2(OH)2CO3,有四种元素组成不属于氧化物;
Ⅱ.(1)由炼铁高炉中反应可知,碳首先燃烧生成二氧化碳放出大量的热量,可供还原铁矿石提供热量,然后和焦炭反应生成CO,然后再还原还原铁矿石.所以,焦炭的作用是燃烧提供能量和制取CO;生成铁的反应是:Fe2O3+3CO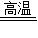 2Fe+3CO2;
2Fe+3CO2;
(2)①一氧化碳具有还原性,可与氧化铁反应生成黑色的铁和二氧化碳.所以,实验中玻璃管里固体粉末的颜色变化是红色粉末逐渐变黑;生成的二氧化碳能与氢氧化钙反应生成了碳酸钙沉淀和水,反应的方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;
②由于该反应的尾气中含有一氧化碳,有毒能污染空气.所以,该装置的缺陷是:没有进行尾气处理;
(3)①由质量守恒定律可知,玻璃管中固体减少的质量是氧化铁中氧元素的质量,即7.2g-6g=1.2g,剩余的固体是铁粉,质量为6g.所以,该混合物中铁元素与氧元素的质量比是:6g:1.2g=5:1.
②氧化铁的质量为: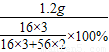 =4g.
=4g.
该混合物中铁粉的质量分数是: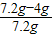 ×100%=44.4%.
×100%=44.4%.
故答为:Ⅰ.B;Ⅱ.(1)制取还原剂CO,3CO+Fe2O3 2Fe+3CO2;(2)①红色粉末逐渐变黑,CO2+Ca(OH)2=CaCO3↓+H2O;②没有进行尾气处理;(3)①混合物中铁元素与氧元素的质量比是5:1; ②该混合物中铁粉的质量分数44.4%.
2Fe+3CO2;(2)①红色粉末逐渐变黑,CO2+Ca(OH)2=CaCO3↓+H2O;②没有进行尾气处理;(3)①混合物中铁元素与氧元素的质量比是5:1; ②该混合物中铁粉的质量分数44.4%.
点评:本题考查了一氧化碳还原氧化铁的反应原理、步骤、实验现象、尾气处理以及应用.要注意有毒气体不能随意排放,必须经过处理后变成无害物质再排放.
Ⅱ.(1)根据炼铁炉内发生的反应,分析焦炭的作用和写出有铁生成的化学方程式;
(2)①一氧化碳具有还原性,可与氧化铁反应生成黑色的铁和二氧化碳,二氧化碳能与氢氧化钙反应生成了碳酸钙沉淀和水.据此分析回答;
②根据尾气中含有一氧化碳,有毒能污染空气分析;
(3)①根据质量守恒定律分析计算混合物中铁元素与氧元素的质量比;
②根据化学式,由氧元素的质量求出氧化铁的质量,即可求出铁粉的质量,再求出混合物中铁粉的质量分数.
解答:解:Ⅰ、由矿石的成分可知,孔雀石的主要成分是Cu2(OH)2CO3,有四种元素组成不属于氧化物;
Ⅱ.(1)由炼铁高炉中反应可知,碳首先燃烧生成二氧化碳放出大量的热量,可供还原铁矿石提供热量,然后和焦炭反应生成CO,然后再还原还原铁矿石.所以,焦炭的作用是燃烧提供能量和制取CO;生成铁的反应是:Fe2O3+3CO
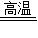 2Fe+3CO2;
2Fe+3CO2;(2)①一氧化碳具有还原性,可与氧化铁反应生成黑色的铁和二氧化碳.所以,实验中玻璃管里固体粉末的颜色变化是红色粉末逐渐变黑;生成的二氧化碳能与氢氧化钙反应生成了碳酸钙沉淀和水,反应的方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;
②由于该反应的尾气中含有一氧化碳,有毒能污染空气.所以,该装置的缺陷是:没有进行尾气处理;
(3)①由质量守恒定律可知,玻璃管中固体减少的质量是氧化铁中氧元素的质量,即7.2g-6g=1.2g,剩余的固体是铁粉,质量为6g.所以,该混合物中铁元素与氧元素的质量比是:6g:1.2g=5:1.
②氧化铁的质量为:
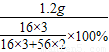 =4g.
=4g.该混合物中铁粉的质量分数是:
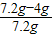 ×100%=44.4%.
×100%=44.4%.故答为:Ⅰ.B;Ⅱ.(1)制取还原剂CO,3CO+Fe2O3
 2Fe+3CO2;(2)①红色粉末逐渐变黑,CO2+Ca(OH)2=CaCO3↓+H2O;②没有进行尾气处理;(3)①混合物中铁元素与氧元素的质量比是5:1; ②该混合物中铁粉的质量分数44.4%.
2Fe+3CO2;(2)①红色粉末逐渐变黑,CO2+Ca(OH)2=CaCO3↓+H2O;②没有进行尾气处理;(3)①混合物中铁元素与氧元素的质量比是5:1; ②该混合物中铁粉的质量分数44.4%.点评:本题考查了一氧化碳还原氧化铁的反应原理、步骤、实验现象、尾气处理以及应用.要注意有毒气体不能随意排放,必须经过处理后变成无害物质再排放.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
