题目内容
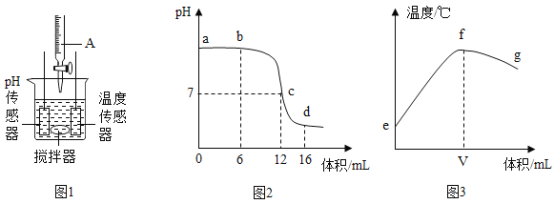
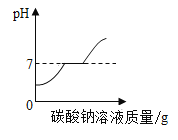
【题目】(1)用稀硫酸和氢氧化钠溶液进行中和反应实验时,反应过程溶液pH变化曲线如图所示:
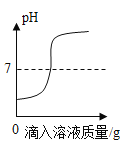
该实验操作是将________(写溶质的化学式)溶液逐滴加入到另一种溶液中。
(2)当滴加的溶液到一定量并充分反应时,请对烧杯中溶质成分进行探究。
(提出问题)此时烧杯中的溶质成分是什么?
(猜想与假设)Ⅰ:Na2SO4 Ⅱ:_______ Ⅲ:Na2SO4和NaOH
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
取少量上述烧杯中的溶液与试管中,滴加_________溶液 | ________ | 猜想Ⅲ不正确 |
载取少量上述烧杯中的溶液与试管中,加入适量的________ | 有气泡产生 | 猜想Ⅱ正确 |
(拓展与延伸)(1)若要猜想Ⅱ成立,还可以单独用下列______(填字母)得出此结论;
A Cu B石蕊试液 C BaCl2 D CuO
(2)在分析反应后所得物质的成分时,除考虑生成物外,还需考虑_______
【答案】NaOH Na2SO4和H2SO4 无色酚酞(硫酸铜溶液或三氯化铁溶液) 无现象 锌(铁、镁、大理石、碳酸钠) B D 反应物是否过量
【解析】
(1)由图可知溶液由酸性变为碱性,故滴加的应是是碱氢氧化钠,故填:NaOH;
(2)[猜想与假设]氢氧化钠和硫酸反应;有可能恰好完全反应,溶质是Na2SO4;有可能酸过量,溶质是Na2SO4和H2SO4;再或者氢氧化钠过量溶质是Na2SO4和NaOH;故填:Na2SO4和H2SO4。
[实验探究]证明猜想Ⅲ不正确,只需要证明不含NaOH,不含氢氧化钠的话,滴加无色酚酞(硫酸铜溶液或三氯化铁溶液),无现象;证明猜想Ⅱ正确只需要证明含H2SO4,有H2SO4的话加入锌(铁、镁、大理石、碳酸钠)会产生气泡,故填:无色酚酞(硫酸铜溶液或三氯化铁溶液);无现象;锌(铁、镁、大理石、碳酸钠)。
[延伸与拓展] (1)证明猜想Ⅱ正确只需要证明含H2SO4:
A、Cu和硫酸不反应,不能证明含H2SO4,不符合题意。
B、石蕊试液遇H2SO4会变红,没有H2SO4石蕊试液不会变色,可通过现象鉴别是否有H2SO4符合题意。
C、硫酸钠和氯化钡生成硫酸钡沉淀和氯化钠,硫酸和氯化钡生成硫酸钡沉淀和氯化氢,无论是否有硫酸滴加氯化钡都会产生白色沉淀,不符合题意。
D、氧化铜和硫酸反应,固体会溶解,溶液变蓝色,可通过现象鉴别是否有H2SO4符合题意。
故选:BD。
(2)在分析反应后所得物质的成分时,除考虑生成物外,还需考虑反应物是否过量,故填:反应物是否过量。

 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案