题目内容
【题目】(7分)下图为实验室中常见的气体制备、净化、收集和性质实验的部分仪器。
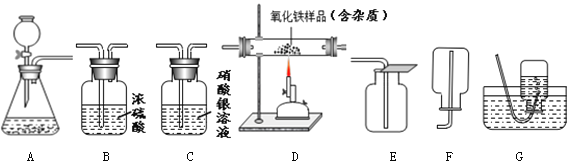
(1)若以二氧化锰和过氧化氢溶液为原料制取氧气,现要收集一瓶干燥的氧气。
①所选仪器的连接顺序为 (填写装置序号字母)。
②制取氧气时,装置A中发生反应的化学方程式为 。
(2)利用该套装置还可以在实验室制取二氧化碳,石灰石和稀盐酸反应后,剩余废液中常含有少量盐酸。若要检验该废液中是否含有盐酸,请你从“硝酸银溶液、酚酞试液、pH试纸、熟石灰”中选用一种进行实验,并简述实验过程 。
(3)若装置A中盛放锌粒和稀盐酸,小明同学欲利用制备的氢气来测定10 g氧化铁样品中氧化铁的纯度(杂质不反应),仪器连接顺序为:A→C→B1→D→B2→B3。(已知:Fe2O3 + 3H2 高温 2Fe + 3H2O ,其中B1、B2、B3为3个浓硫酸洗气瓶)
①连接仪器C的目的是 。
②若装置中不连接B1,用B2装置在反应前后质量的增加进行计算,则计算结果会 (选填“偏大”、“偏小”、“不受影响”之一)。
③若测得B2增加的质量为a g,则该样品中氧化铁的质量分数为 (可为分数形式)。
【答案】(1)①A- B-E ②2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。
(2)pH试纸。(1分)用玻璃棒或胶头滴管把待测液滴到pH试纸上,变色后,立即与标准比色卡比较读数,即得溶液的pH(1分)。
(3)①除去氢气中的HCl气体 ② 偏大 ③ 8a/27
【解析】
试题分析:(1)若以二氧化锰和过氧化氢溶液为原料制取氧气,现要收集一瓶干燥的氧气,应该干燥气体,同时用向上排空气法收集,故① 所选仪器的连接顺序为A- B-E;② 制取氧气时,装置A中发生反应的化学方程式为2H2O2![]() 2H2O+O2↑。(2)检验该废液中是否含有盐酸,只能检验氢离子的存在,最好的方法为选用PH试纸,其操作为用玻璃棒或胶头滴管把待测液滴到pH试纸上,变色后,立即与标准比色卡比较读数,即得溶液的pH;(3)①连接仪器C的目的是除去氢气中的HCl气体; ② 若装置中不连接B1,用B2装置在反应前后质量的增加进行计算,则计算结果会偏大,原因为水蒸气被B2吸收,造成生成水的质量增大,故计算结果偏大;③ 若测得B2增加的质量为a g,设氧化铁的质量为X;根据Fe2O3 + 3H2 高温 2Fe + 3H2O
2H2O+O2↑。(2)检验该废液中是否含有盐酸,只能检验氢离子的存在,最好的方法为选用PH试纸,其操作为用玻璃棒或胶头滴管把待测液滴到pH试纸上,变色后,立即与标准比色卡比较读数,即得溶液的pH;(3)①连接仪器C的目的是除去氢气中的HCl气体; ② 若装置中不连接B1,用B2装置在反应前后质量的增加进行计算,则计算结果会偏大,原因为水蒸气被B2吸收,造成生成水的质量增大,故计算结果偏大;③ 若测得B2增加的质量为a g,设氧化铁的质量为X;根据Fe2O3 + 3H2 高温 2Fe + 3H2O
160 54
X a
160/x=54/a
X=160a/54
则该样品中氧化铁的质量分数为160a/54×10=8a/27。
