题目内容
2012年4月15日,央视《每周质量报告》报道:一些不法企业用皮革废料熬制的工业明胶生产药用胶囊。在熬制明胶过程中添加重铬酸钾(K2Cr2O7) ,导致生产的药用胶囊重金属铬超标。根据化学式计算:
,导致生产的药用胶囊重金属铬超标。根据化学式计算:
(1)该物质由 种元素组成。
(2)钾、铬、氧三种元素的质量比为 (要求填最简整数比)。
(3)铬元素的质量分数为 (结果保留到0.1%)。
(4)29 .4 g该物质中含有钾元素的质量为 g。
.4 g该物质中含有钾元素的质量为 g。
(1)三(或3) (2)39∶52∶56 (3)35.4% (4)7.8
解析:(1)重铬酸钾是由钾、铬、氧三种元素组成 的;(2)重铬酸钾中钾、铬、氧三种元素的质量比=(39×2)∶(52×2)∶(16×7)=39∶52∶56;(3)重铬酸钾中铬元素的质量分数=
的;(2)重铬酸钾中钾、铬、氧三种元素的质量比=(39×2)∶(52×2)∶(16×7)=39∶52∶56;(3)重铬酸钾中铬元素的质量分数=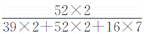 ×100%≈35.4%;(4)29.4 g该物质中含有钾元素的质量=29.4 g×
×100%≈35.4%;(4)29.4 g该物质中含有钾元素的质量=29.4 g×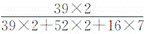 ×100%=7.8 g。
×100%=7.8 g。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 (2012?海南)2012年4月15日,中央电视台曝光一些药企用工业明胶制作胶囊,引发了人们对铬元素的关注,在元素周期表中铬元素部分信息如图所示,下列说法中错误的是( )
(2012?海南)2012年4月15日,中央电视台曝光一些药企用工业明胶制作胶囊,引发了人们对铬元素的关注,在元素周期表中铬元素部分信息如图所示,下列说法中错误的是( )
 2012年4月15日,央视《每周质量报告》报道一些企业用皮革废料熬制工业明胶,在加工过程中添加重铬酸钾,导致工业明胶制造的药用胶囊中重金属铬超标.铬在人体内能对肝、肾等内脏器官和DNA造成损伤.如图是铬元素在元素周期表中的一格,你不能从该图得到的信息有( )
2012年4月15日,央视《每周质量报告》报道一些企业用皮革废料熬制工业明胶,在加工过程中添加重铬酸钾,导致工业明胶制造的药用胶囊中重金属铬超标.铬在人体内能对肝、肾等内脏器官和DNA造成损伤.如图是铬元素在元素周期表中的一格,你不能从该图得到的信息有( )