题目内容
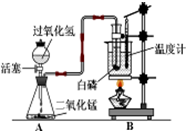 某学校化学学习小组设计出如图所示装置,并进行白磷燃烧实验.
某学校化学学习小组设计出如图所示装置,并进行白磷燃烧实验.(1)当烧杯内的水受热,温度计显示30℃时,打开活塞,在盛有水的试管中有气泡均匀逸出,白磷未燃烧,关闭活塞.锥形瓶内反应的化学方程式是:
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.白磷未燃烧的原因是
| ||
温度未达到白磷的着火点
温度未达到白磷的着火点
.(2)随着水温升高,温度计显示45℃时,再次打开活塞,白磷在水里燃烧.常言道,水火不相容.水能灭火的原因是
可以使可燃物温度降至着火点以下和隔绝氧气
可以使可燃物温度降至着火点以下和隔绝氧气
.而本实验中白磷在水里还能够燃烧的原因是温度达到着火点,同时又与氧气充分接触
温度达到着火点,同时又与氧气充分接触
.(3)本实验装置的A部分还可以用于制取的气体是
二氧化碳
二氧化碳
,收集方法是向上排空气法
向上排空气法
;化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
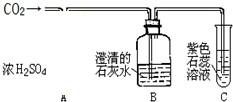
.(4)下图是某同学设计的验证CO2化学性质的实验装置.请回答:装置B在初中化学中常用来检验CO2气体,是因为CO2能使澄清的石灰水
变浑浊
变浑浊
;化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O
CO2+Ca(OH)2═CaCO3↓+H2O
.实验过程中,在C处可观察到紫色石蕊溶液变红色
变红色
.化学方程式为CO2+H2O═H2CO3
CO2+H2O═H2CO3
.
分析:(1)物质燃烧需要同时具备三个条件,即物质具有可燃性、与氧气接触、温度达到可燃物的着火点;
(2)使可燃物与氧气隔绝或降低温度到可燃物的着火点以下可以达到灭火的目的;
(3)根据反应物和生成物及其质量守恒定律可以书写化学方程式,根据反应物和生成物的性质可以选择实验装置和收集气体的方法.
(4)依据二氧化碳与氢氧化钙的反应以及与水的反应分析判断即可.
(2)使可燃物与氧气隔绝或降低温度到可燃物的着火点以下可以达到灭火的目的;
(3)根据反应物和生成物及其质量守恒定律可以书写化学方程式,根据反应物和生成物的性质可以选择实验装置和收集气体的方法.
(4)依据二氧化碳与氢氧化钙的反应以及与水的反应分析判断即可.
解答:解:(1)过氧化氢在二氧化锰的作用下反应能生成水和氧气,化学方程式为:2H2O2
2H2O+O2↑,白磷的着火点是40℃,白磷未燃烧的原因是温度未达到白磷的着火点.
(2)水能灭火的原因是:水可以使可燃物温度降至着火点以下并且能够隔绝氧气,磷在水里还能够燃烧的原因是温度达到着火点,同时又与氧气充分接触.
(3)实验室制取二氧化碳或氢气时,不需要加热,可以用本实验装置的A部分制取,二氧化碳的密度比空气大,可以用向上排空气法收集,其方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(4)由于二氧化碳与氢氧化钙反应生成碳酸钙,所以变浑浊.由于氢氧化钙对二氧化碳的吸收能力很差,所以气体进入C,二氧化碳与水反应生成碳酸能使紫色石蕊试液变红.
故答案为:(1)2H2O2
2H2O+O2↑.温度未达到白磷的着火点(2)可以使可燃物温度降至着火点以下并且能够隔绝氧气;温度达到着火点,同时又与氧气充分接触
(3)二氧化碳;向上排空气法;CaCO3+2HCl═CaCl2+H2O+CO2↑.(4)变浑浊;CO2+Ca(OH)2═CaCO3↓+H2O;变红色;CO2+H2O═H2CO3
| ||
(2)水能灭火的原因是:水可以使可燃物温度降至着火点以下并且能够隔绝氧气,磷在水里还能够燃烧的原因是温度达到着火点,同时又与氧气充分接触.
(3)实验室制取二氧化碳或氢气时,不需要加热,可以用本实验装置的A部分制取,二氧化碳的密度比空气大,可以用向上排空气法收集,其方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(4)由于二氧化碳与氢氧化钙反应生成碳酸钙,所以变浑浊.由于氢氧化钙对二氧化碳的吸收能力很差,所以气体进入C,二氧化碳与水反应生成碳酸能使紫色石蕊试液变红.
故答案为:(1)2H2O2
| ||
(3)二氧化碳;向上排空气法;CaCO3+2HCl═CaCl2+H2O+CO2↑.(4)变浑浊;CO2+Ca(OH)2═CaCO3↓+H2O;变红色;CO2+H2O═H2CO3
点评:解答本题要根据质量守恒定律书写化学方程式,要充分理解燃烧的条件和灭火的方法,同时还要理解制取气体的实验装置和收集气体的方法,这些都是解题的关键.

练习册系列答案
相关题目
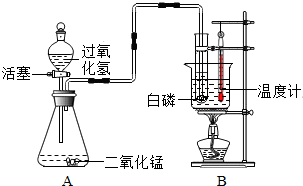 某学校化学学习小组设计出如图所示装置,并进行白磷燃烧实验.
某学校化学学习小组设计出如图所示装置,并进行白磷燃烧实验.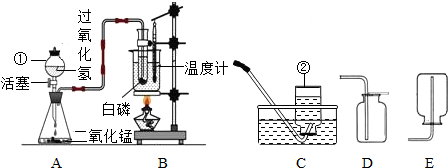
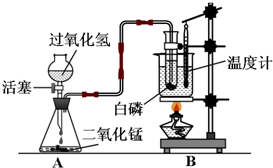 某学校化学学习小组设计出右图所示装置,并进行白磷燃烧实验.
某学校化学学习小组设计出右图所示装置,并进行白磷燃烧实验. 某学校化学学习小组设计出如图所示装置,并进行白磷燃烧实验.
某学校化学学习小组设计出如图所示装置,并进行白磷燃烧实验.