题目内容
【题目】金属在生产和生活中具有广泛的应用。
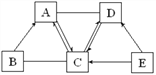
(1)如图的金属制品中,主要利用金属导电性的是_____________(填字母序号)

(2)为了保护有限的金属资源,下列措施合理的是____________
A.回收铝制饮料罐
B.在铁制品表面刷漆、涂油,防止生锈
C.尽量将已探明的铁矿石全部开采出来 D.积极研发新材料以替代金属材料
(3)应用金属活动性顺序能帮助我们进一步学习金属性质。已知下列各组物质间均能发生化学反应。
A.Fe和CuSO4溶液 B.Mg和MnSO4溶液 C.Mn和FeSO4溶液
①写出Fe和CuSO4溶液反应的化学方程式____
②以上四种金属的活动性强弱由强到弱的顺序是_______
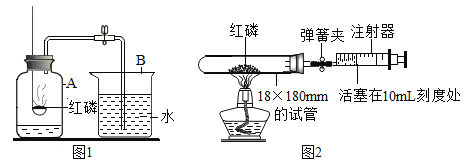
(4)化学小组对含有硫酸铜和硫酸锌的废液进行了如所示的处理:

①步骤I中的操作名称是________
②滤液的成分中一定含有的金属阳离子是__________(填序号)
【答案】B ABD Fe+CuSO4═FeSO4+Cu Mg>Mn>Fe>Cu 过滤 Zn2+、Fe2+
【解析】
(1)根据金属的性质进行分析;
(2)根据保护金属资源的措施分析;
(3)根据金属的活动性进行分析;
(4)根据实验操作和金属的化学性质进行分析.
(1)根据金属的导电性和三个选项分析可知,铁锅主要利用了金属的导热性,铜导线利用了铜具有良好的导电性,水龙头主要应用了金属的硬度大。故选B;
(2)由于保护有限的金属资源,有很多可取的方法,回收、防止金属生锈、积极研发替代材料等,故选ABD;
(3)铁能把铜从硫酸铜中置换出来,化学方程式为:Fe+CuSO4═FeSO4+Cu;
Fe和CuSO4溶液能反应,说明Fe>Cu;Mg和MnSO4溶液能反应,说明Mg>Mn;Mn和FeSO4溶液能反应说明Mn>Fe。这四种金属的活动性顺序为:Mg>Mn>Fe>Cu;
(4)过滤能将固体与液体分离,根据实验操作进行分析可知,操作Ⅰ是过滤,在金属活动性顺序中,Zn>Fe>Cu,在硫酸铜和硫酸锌的溶液中加入铁粉,只有铁与硫酸铜溶液反应生成硫酸亚铁和铜,滤渣加入稀硫酸没有气体产生,说明不含有铁,所以滤渣中一定含有铜,滤液中一定含有硫酸锌和硫酸亚铁,滤液的成分中一定含有的金属阳离子是Zn2+、Fe2+。

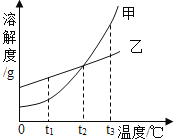
【题目】学习了二氧化锰对过氧化氢有催化作用的知识后,某同学想:氧化铜(CuO)能否起到类似二氧化锰的作用呢?进行了如下探究。(猜想)Ⅰ.CuO参与反应产生氧气,反应前后质量和化学性质发生了改变; Ⅱ.CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;Ⅲ.CuO是反应的催化剂,反应前后_______________________不变。(实验)用天平称量0.2gCuO,取5mL 5%的过氧化氢溶液于试管中,进行如下实验:
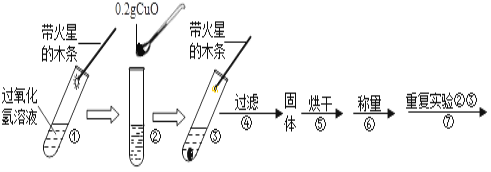
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
溶液中有气泡放出, 带火星的木条复燃 | _________________ | _________________ | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
(2)步骤①的目的_______________________。
(3)过氧化氢能被氧化铜催化分解放出氧气的反应文字表达式为__________________。
(4)查阅资料知氧化铁、硫酸铜、猪肝等也可以作过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是_______(填字母代号)
A.用作催化剂的物质不可能是其他反应的反应物或生成物
B.一种物质无法对多个反应都起催化作用
C.同一化学反应可以有多种催化剂
D.催化剂能使生成氧气的质量增加
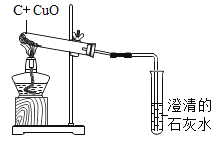
【题目】下图是制取二氧化碳并进行有关物质的性质实验的装置。请根据要求回答有关问题。
查阅资料可知:氢氧化钠可以吸收二氧化碳,反应的方程式为:CO2+2NaOH=Na2CO3+H2O
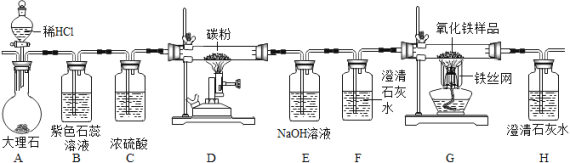
(1)写出下列装置中的化学方程式:装置A:______,装置G__________
(2)实验过程中装置B中的现象是_________装置F的作用是_______
(3)将A中的稀盐酸不断滴入大理石后,应先点燃_________(选填D或G处)的酒精灯。
(4)充分反应前后G装置的质量分别表示于右下表中,则样品中氧化铁的的质量为_____g
G | |
反应前(g) | 57.8 |
反应后(g) | 55.4 |
(5)该装置有一处明显的不足,请你给出改进的具体措施_________
【题目】下图为元素A的原子的结构示意图,请回答:

(1)该原子的原子核中有_____个质子,_______个中子。
(2)下表为元素周期表中部分元素的信息,可知A的元素符号为_________,该元素形成的氧化物的化学式为__________。
第2周期 | 3Li 锂 6.941 | 4Be 铍 9.012 | 5B 硼 10.81 | 6C 碳 12.01 | 7N 氮 14.01 | 8O 氧 16.00 | 9F 氟 19.00 | 10Ne 氖 20.18 |
(3)以碳12原子的质量1.993×10—26kg,一种铁原子的质量为9.288×10—26kg,计算该铁原子的相对原子质量为___________________(只列出计算式)。