题目内容
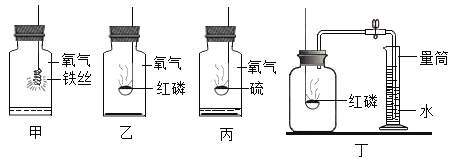
【题目】请根据如图所示的实验装置图填空。
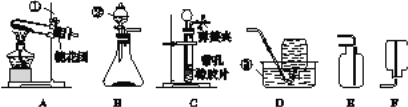
(1)指出图中标有数字的仪器的名称:①__________,②____________,③____________。
(2)在实验室用高锰酸钾制氧气时,试管口的棉花团的作用是___________________,
写出反应的文字表达式:________________。
(3)当实验室中用B装置制取氧气时,仪器②的作用是___________、___________,该反应的文字表达式为________________。
(4)在实验室制取并收集二氧化碳可选用______________(填序号)装置,写出实验室制取二氧化碳的文字表达式:____________。
(5)检查装置B气密性的方法是_________,装置C相对于装置B在操作方面的优势为_______。
(6)某位同学设计了如图所示五套制取二氧化碳的装置,其中能达到装置C操作优势的是________(填序号)。
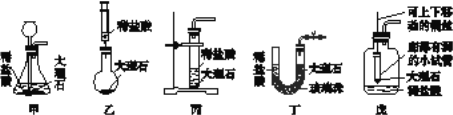
(7)在实验室中常用加热醋酸钠和碱石灰的固体混合物来制取甲烷气体。甲烷是一种无色无味、密度比空气小、极难溶于水的气体, 则制取并收集甲烷,应该从图A~F中选择的发生装置是________(填序号),收集装置是______________(填序号)。
(8)若用如图所示装置进行向上排空气法收集氧气的实验,气体应从_____(填“a”或“b”)端导入。
![]()
【答案】铁架台分液漏斗水槽防止高锰酸钾粉末进入导管高锰酸钾![]() 锰酸钾+二氧化锰+氧气滴加过氧化氢溶液控制反应的速率过氧化氢
锰酸钾+二氧化锰+氧气滴加过氧化氢溶液控制反应的速率过氧化氢![]() 水+氧气BE或CE碳酸钙+盐酸―→氯化钙+水+二氧化碳关闭分液漏斗活塞,将导管一端浸入水中,双手紧贴锥形瓶外壁,导管口冒气泡,表明装置不漏气可控制反应的发生与停止丁、戊AD或Fa
水+氧气BE或CE碳酸钙+盐酸―→氯化钙+水+二氧化碳关闭分液漏斗活塞,将导管一端浸入水中,双手紧贴锥形瓶外壁,导管口冒气泡,表明装置不漏气可控制反应的发生与停止丁、戊AD或Fa
【解析】
⑴①仪器为铁架台;②仪器为分液漏斗;③仪器为水槽;
⑵加热高锰酸钾制氧气,试管口塞棉花团的作用是:防止高锰酸钾粉末进入导管;反应的文字表达式为:高锰酸钾![]() 锰酸钾+二氧化锰+氧气;
锰酸钾+二氧化锰+氧气;
⑶用B装置制取氧气的原理是:过氧化氢在二氧化锰的催化下分解生成水和氧气,因此仪器②的作用是:滴加过氧化氢溶液,且分液漏斗可以通过调节过氧化氢的滴速来控制反应的速率;该反应的文字表达式为: 过氧化氢![]() 水+氧气;
水+氧气;
⑷实验室制取二氧化碳气体是用大理石和稀盐酸反应,因此发生装置可选择B或C,收集二氧化碳的最好的方法是向上排空气法,因此选E装置;实验室制取二氧化碳的文字表达式为:碳酸钙+盐酸―→氯化钙+水+二氧化碳;
⑸检查装置气密性的方法为捂气法,具体操作为:关闭分液漏斗活塞,将导管一端浸入水中,双手紧贴锥形瓶外壁,导管口冒气泡,表明装置不漏气 ;装置C和B装置的不同是C装置中有一个带孔橡胶片,当把稀盐酸通过长颈漏斗滴入试管中时,稀盐酸没过橡胶板接触到橡胶板上的大理石时可以开始反应,产生二氧化碳,当夹住导管上的试管夹时,反应仍然继续发生,产生的二氧化碳气体不能导出,于是把稀盐酸压回长颈漏斗中,盐酸和大理石无法接触,不再反应,因此可以控制反应的进行与停止,而B装置则没有这样的作用;
⑹丁装置可通过试管夹控制气压来控制稀盐酸和大理石的接触,与装置C原理相同,戊装置可以通过移动小试管控制大理石和稀盐酸的接触进而控制反应的发生与停止;
⑺固体加热的发生装置选A,甲烷密度比空气小,可以选择向下排空气法收集,甲烷极难溶于水,可用排水法收集,可选的装置为D或F;
⑻氧气密度大于空气,所以选用向上排空气法收集,氧气应该从长管进。

【题目】目前全世界的镍(Ni)消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。可以说镍行业发展蕴藏着巨大的潜力。
Ⅰ制备草酸镍
工业上可利用含镍合金废料(除镍外,还含有Fe、Cu、Ca、Mg、C等杂质)制取草酸镍(NiC2O4)。
根据下列工艺流程图回答问题:
(资料卡片1)
(1)过氧化氢(H2O2)俗称双氧水,是一种液体,受热易分解,可用于实验室制取氧气;过氧化氢具有强氧化性,所以常作为氧化剂、漂白剂和消毒剂。
(2)氧化反应可以从元素化合价升降的角度进行物质所含元素化合价升高的反应就是氧化反应。
(3)金属镍的化学性质类似于铁,与盐酸反应能生成氯化镍(NiCl2)。
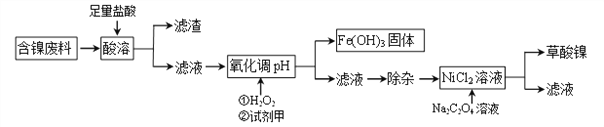
(1)“酸溶”之后的滤渣中含有的金属是_______________。
(2)写出酸溶过程中Ni与盐酸反应的化学方程式_________________________。
(3)加H2O2时,温度不能太高,其原因是_______________________。若H2O2在“酸溶”步骤即与盐酸同时加入,则与原方案相比滤液中会增加的金属离子是Cu2+和_______(写离子符号)。
(4)已知Na2C2O4溶液加入NiCl2溶液发生复分解反应,写出该反应的化学方程式____________。
Ⅱ制备镍粉
工业用电解镍液(主要含NiSO4)制备碱式碳酸镍晶体xNiCO3yNi(OH)2zH2O,并利用其制备镍粉,过程如下:
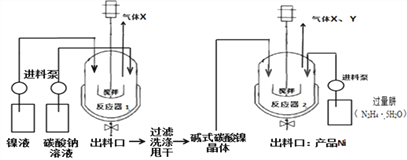
(5)反应器1中的一个重要反应为3NiSO4+3Na2CO3+2H2O ![]() NiCO32Ni(OH)2+3Na2SO4+2X,X的化学式为_________。
NiCO32Ni(OH)2+3Na2SO4+2X,X的化学式为_________。
(6)反应器1的出料口获得的固体洗涤时,需用纯水洗涤,可以用来检验固体已洗涤干净的试剂是____________。
(7)反应器2中产生的气体Y是空气中含量最多的气体,该气体是_________(填名称)。
Ⅲ 测定碱式碳酸镍晶体的组成
为测定碱式碳酸镍晶体(xNiCO3yNi(OH)2zH2O)组成,某小组设计了如下实验方案及装置:
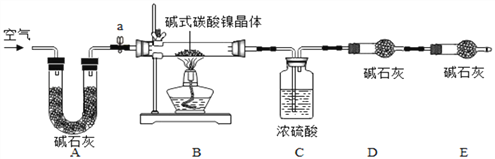
(资料卡片2)
(1)碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O
(2)在温度控制不当导致温度过高时,NiO会被氧化成Ni2O3
(3)碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O
(实验步骤)
①检查装置气密性;②准确称取3.77g碱式碳酸镍晶体(xNiCO3yNi(OH)2zH2O)放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,分别称量装置C、D、E的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,缓缓鼓入一段时间空气;⑥分别准确称量装置C、D、E的质量;⑦根据数据进行计算(相关数据如下表)。
装置C/g | 装置D/g | 装置E/g | |
加热前 | 200.00 | 180.00 | 180.00 |
加热后 | 201.08 | 180.44 | 180.00 |
(实验分析及数据处理)
8)实验过程中步骤⑤鼓入空气的目的是__________________。
(9)计算3.77g碱式碳酸镍晶体(xNiCO3yNi(OH)2zH2O)中镍元素的质量_________(写出计算过程,计算结果准确到小数点后两位)。
(实验反思)
(10)另一小组同学在实验中发现,实验结束后,称得装置B中残留固体质量明显偏大,老师带领全组同学经过仔细分析后发现,这是由于该组同学加热时在酒精灯上加了铁丝网罩,温度过高所导致。请问该组同学称得的残留固体中镍元素的质量分数可能是__________。
A.70.08% B.75.88% C.78.67% D.79.58%
【题目】某校研究性学习小组的同学为了探究人呼出的气体与吸入的空气中氧气、二氧化碳和水蒸气的含量是否相同,设计了简单的实验方案,其主要操作步骤如图所示。请根据图示回答下列问题。
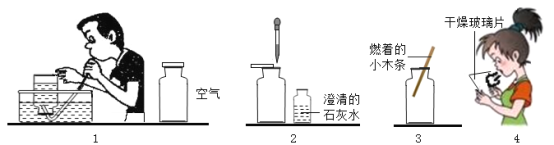
(1)图中收集呼出气体的方法是____________。
(2)下表是他们的探究方案,请你填写完整。
探究内容 | 实验方法 | 判断依据 |
二氧化碳含量是否相同 | ______ | ______ |
氧气含量是否相同 | ______ | ______ |
水蒸气含量是否相同 | ______ | ______ |
(3)结论:___________________。