题目内容
取粉末状大理石样品和块状大理石样品各12克,分别与足量的稀盐酸在烧杯中混合后充分反应,测得反应生成气体的质量(m)与反 应时间(t)的数据如下表所示:
应时间(t)的数据如下表所示:
| 实验序号 | 反应时间t/s | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 |
| ① | 气体质量m/ | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.40 | 4.40 | 4.40 | 4.40 |
| ② | 气体质量m/g | 0 | 0.42 | 1.42 | 2.30 | 3.32 | 4.20 | 4.38 | 4.40 | 4.40 |
回答问题:
Ⅰ.粉末状大理石和盐酸反应所对应的实验序号是 (15) (填“①”或“②”)。
Ⅱ.求实验①中参加反应的碳酸钙的物质的量(用化学方程式计算)
Ⅲ.实验①中大理石样品的纯度(即大理石中碳酸钙的质量分数)为 (16) 。
(16) 。
(精确到0.1%)
Ⅰ① ; Ⅱ n(C O2 )=4.4g/44g/mol=0.1mol ———————1分 。
O2 )=4.4g/44g/mol=0.1mol ———————1分 。
设碳酸钙 的物质的量xmol
的物质的量xmol
CaCO3 +2HCl→CaCl2 +H2O +CO2↑ ———————1分
1 1
xmol 0.1mol
 =
=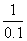 ———————1分
———————1分
x =0.1mol ———————1分
Ⅲ大理石样品的纯度=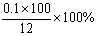 = 83.3%(1分)
= 83.3%(1分)

取粉末状大理石样品和块状大理石样品各12克,分别与足量的稀盐酸在烧杯中混合后充分反应,测得反应生成气体的质量(m)与反 应时间(t)的数据如下表所示:
应时间(t)的数据如下表所示:
| 实验序号 | 反应时间t/s | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 |
| ① | 气体质量m/ | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.40 | 4.40 | 4.40 | 4.40 |
| ② | 气体质量m/g | 0 | 0.42 | 1.42 | 2.30 | 3.32 | 4.20 | 4.38 | 4.40 | 4.40 |
回答问题:
Ⅰ.粉末状大理石和盐酸反应所对应的实验序号是 (15) (填“①”或“②”)。
Ⅱ.求实验①中参加反应的碳酸钙的物质的量(用化学方程式计算)
Ⅲ.实验①中大理石样品的纯度(即大理石中碳酸钙的质量分数)为 (16) 。
(16) 。
(精确到0.1%)
 g
g g
g