题目内容
【题目】将某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的甲、乙两种金属,反应后金属都没有剩余。产生H2的质量随时间变化的关系如图所示。下列说法错误的是
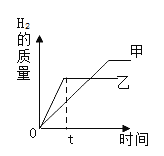
A.O~t时间段内,乙产生氢气的速率比甲快
B.如果形成的化合物中两种金属元素的化合价相同,则甲的相对原子质量一定比乙小
C.反应消耗H2SO4的质量相等;
D.反应消耗金属的质量相等
【答案】C
【解析】
A. O~t时间段内,相等时间内,乙产生氢气比甲多,故乙产生氢气的速率比甲快,此选项正确;
B. 由图可知,等质量的甲、乙两种金属完全反应,甲产生的氢气比乙多,如果形成的化合物中两种金属元素的化合价相同,则甲的相对原子质量一定比乙小,此选项正确;
C. 由图可知,等质量的甲、乙两种金属完全反应,产生氢气的质量不相等,故反应消耗H2SO4的质量不相等,此选项错误;
D. 因为加入等质量的甲、乙两种金属,反应后金属都没有剩余,故反应消耗金属的质量相等,此选项正确。
故选C。

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目