题目内容
【题目】实验室有一固体混合物,可能含有Fe2O3、Cu、C、NH4HCO3、NH4Cl、(NH4)2SO4等物质中的一种或几种,某实验小组通过以下两个实验进行检验,请回答相关问题:
已知: ![]()
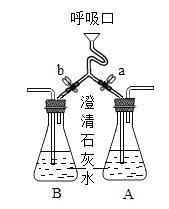
实验一:
(1)由实验一可知:固体混合物中一定没有_______(填名称)。
实验二:
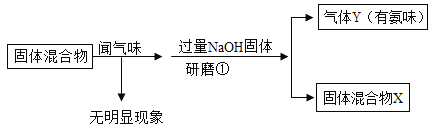
取实验一所得固体混合物X继续实验,流程如下:
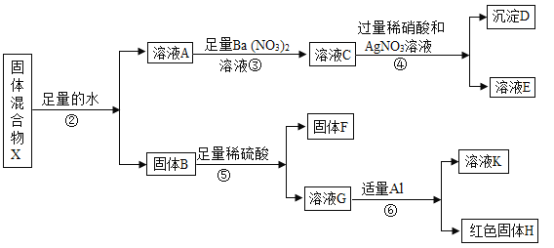
(2)结合实验现象分析,写出步骤①中产生气体Y的化学方程式___________;
(3)写出溶液E中一定含有的溶质_______________(填化学式);
(4)由步骤⑤⑥可知,固体B中一定含有___________(填化学式);
(5)固体F的组成有________ 种情况(填数字)。
【答案】碳酸氢铵 NaOH+NH4Cl═NaCl+H2O+NH3↑ Ba(NO3)2、HNO3、NaNO3 Fe2O3、Cu、C 2
【解析】
(1)碳酸氢铵易分解成氨气,氨气有刺激性气味,由实验一可知:固体混合物中一定没有碳酸氢铵。
(2)溶液A中加入硝酸钡无明显现象,说明没有硫酸根离子,滴加硝酸银生成不容易稀硝酸的白色沉淀,说明有氯离子,原混合物中一定有氯化铵,步骤①中产生气体Y的化学方程式NaOH+NH4Cl═NaCl+H2O+NH3↑;
(3)溶液E中一定含有的溶质是:没有参加反应的硝酸钡和硝酸、生成的硝酸钠,化学式为Ba(NO3)2、HNO3、NaNO3。
(4)根据氧化铁和稀硫酸反应生成硫酸铁和水,![]() ,铝和硫酸铜反应生成铜和硫酸铝,由步骤⑤⑥可知,固体B中一定含有Fe2O3、Cu、C。
,铝和硫酸铜反应生成铜和硫酸铝,由步骤⑤⑥可知,固体B中一定含有Fe2O3、Cu、C。
(5)固体F的组成有2种情况:碳,碳和铜。

 目标测试系列答案
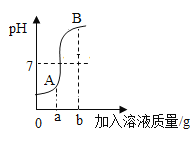
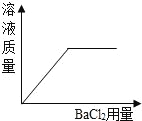
目标测试系列答案【题目】常温下,往盛有一定量液体甲的烧杯中逐渐加人固体乙并充分搅拌。如图所示中横坐标工表示固体乙的质量,纵坐标y表示烧杯中的某物理量(见下表)。下列实验与图像对应关系合理的是
甲 | 乙 | y | |
A | 稀盐酸 | 氧化铜 | 溶液的质量 |
B | 水 | 氢氧化钠 | 溶液的质量 |
C | 饱和石灰水 | 生石灰 | 溶质的质量 |
D | 硝酸银溶液 | 铜粉 | 溶质的质量 |

A.AB.BC.CD.D
【题目】为测定某赤铁矿中氧化铁的质量分数,化学小组同学将12.5 g赤铁矿粉加到烧杯中,并把100 g稀硫酸分四次加入其中(赤铁矿中的其它成分既不溶于水又不和稀硫酸发生反应),每次加入稀硫酸并充分反应后的相关数据如下表。请计算:
实验次数 | 一 | 二 | 三 | 四 |
加入稀硫酸质量/g | 20.0 | 20.0 | 20.0 | 20.0 |
剩余固体质量/g | 8.5 | 4.5 | 2.5 | 2.5 |
(1)实验所用赤铁矿中氧化铁的质量是__。
(2)实验所用稀硫酸中溶质的质量分数___。