题目内容
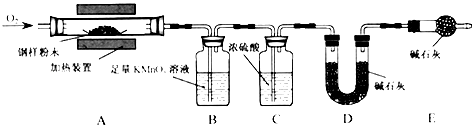
【题目】某工厂以含有FeSO4和少量H2SO4的废水为原料制备FeSO47H2O的步骤如下: ①调节废水pH;②过滤;③蒸发浓缩;④结晶池中结晶;⑤收集晶体,洗涤、干燥.
(1)调节废水pH时,适宜加入 . (填序号) a.Fe b.Cu c.Ca(OH)2
(2)实验室中,完成过滤操作需要的玻璃仪器有玻璃棒、和 , 过滤和蒸发操作中玻璃棒的作用分别是、 .
(3)结晶池底部有一定坡度的主要目的是 .
(4)用冰水洗涤FeSO47H2O晶体的目的是 . 低温干燥的目的是 .
(5)结合如图,补充完整由硫酸亚铁溶液中结晶出FeSO44H2O的实验方案:蒸发浓缩, , 过滤、洗涤、干燥. 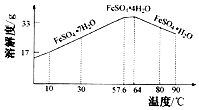
【答案】
(1)a
(2)烧杯;漏斗;引流;搅拌
(3)便于收集晶体
(4)减少晶体因溶解而损失;防止受热晶体失去结晶水
(5)结晶
【解析】解:(1)调节废水pH时,为避免引入新的杂质,在给定的物质中加入Fe是最合适的,故选 a.(2)实验室中,完成过滤操作需要的玻璃仪器有玻璃棒、烧杯和 漏斗,过滤和蒸发操作中玻璃棒的作用分别是 引流、搅拌.(3)结晶池底部有一定坡度,使结晶出来的晶体能够集中在一起,便于收集晶体.(4)由于FeSO47H2O晶体易溶于水,所以在洗涤的时候用冰水洗涤FeSO47H2O晶体减少晶体因溶解而损失.由于FeSO47H2O晶体受热容易失去结晶水,所以采取低温干燥.防止受热晶体失去结晶水.(5)结合如图,补充完整由硫酸亚铁溶液中结晶出FeSO44H2O的实验方案:蒸发浓缩,结晶,过滤、洗涤、干燥. 所以答案是:(1)a;(2)烧杯; 漏斗; 引流; 搅拌.(3)便于收集晶体.(4)减少晶体因溶解而损失. 防止受热晶体失去结晶水.(5)结晶.
【考点精析】本题主要考查了过滤操作的注意事项的相关知识点,需要掌握过滤操作注意事项:“一贴”“二低”“三靠;过滤后,滤液仍然浑浊的可能原因有:①承接滤液的烧杯不干净②倾倒液体时液面高于滤纸边缘③滤纸破损才能正确解答此题.