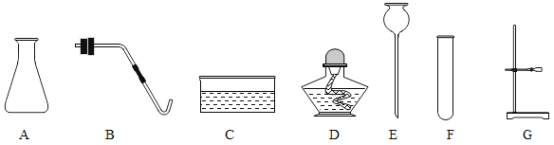
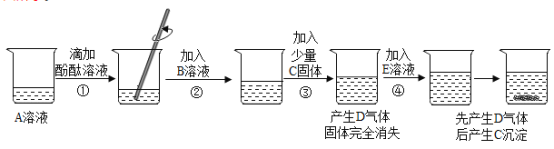
题目内容
短周期(前三周期)元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述不正确的是:
A.X元素可以与W元素形成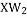 和
和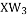 两种化合物
两种化合物
B.Y元素的单质一定条件下可以与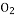 、
、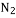 、
、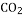 反应
反应
C.Z原子的最外层电子数为4,形成化合物时一般为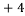
D.X与Y、Z与W都属于同一周期
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案下列实验方案能达到实验目的的是
实验目的 | 实验方案 | |
A | 检验某固体为碳酸盐 | 取样,滴加盐酸,观察是否有气泡 |
B | 证明二氧化碳能与水反应 | 将二氧化碳通入滴有酚酞溶液的水中 |
C | 检验氧气已收集满 | 将带火星的木条伸入集气瓶中 |
D | 证明蜡烛中含有碳元素 | 将内壁蘸有澄清石灰水的烧杯罩在蜡烛火焰上方 |
A.A B.B C.C D.D
碳酸钠是重要的化工原料。吕布兰、索尔维和侯德榜为它的工业化生产作出了巨大贡献。
Ⅰ、吕布兰法:1789年,法国医生吕布兰(N. Leblanc, 1742 -1806)以食盐、浓硫酸、木炭和石灰石为原料,开创了规模化工业制取碳酸钠的先河,具体流程如图:
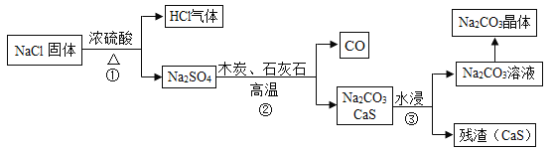
(1)在高温条件下,②中发生两步反应,其中一步是Na2SO4和木炭生成Na2S和CO,该反应的化学方程式为____;
(2)③中”水浸”时通常需要搅拌,其目的是____;
(3)吕布兰法有明显不足,不断有科学家进行改进,请写出该法不足之处__(一处即可)。
II、索尔维法: 1892 年,比利时工程师索尔维发明氨碱法制碳酸钠,又称索尔维法。原理如下:
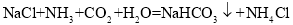
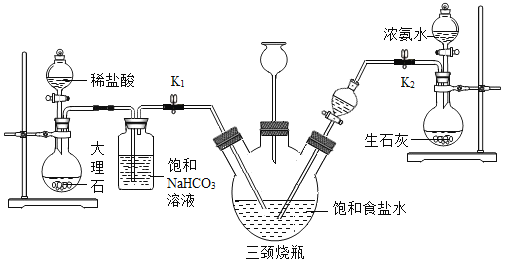
某兴趣小组采用下列装置模拟索尔维法制备碳酸氢钠,进而制得碳酸钠。实验操作如下:
①关闭K1,打开K2,通入NH3,调节气流速率,待其稳定后,打开K1通入CO2;
②三颈烧瓶内出现较多固体时,关闭K2停止通NH3,一段时间后,关闭 K1停止通CO2;
③将三颈烧瓶内的反应混合物过滤、洗涤、低温干燥,并将所得固体置于敞口容器中加热,记录剩余固体质量。
加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 |
剩余固体质量/g | 未记录 | 15.3 | 13.7 | 11.9 | 10.6 | 10.6 |
请回答下列问题:
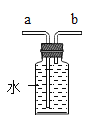
(4)三颈烧瓶上连接的长颈漏斗的主要作用是_______,有同学认为应该在长颈漏斗内放置一团蘸有酸液的棉花,理由是______;关闭K2停止通NH3后,还要继续通CO2一段时间,其目的是_______;
(5)根据实验记录,计算t2时NaHCO3固体的分解率为______( 已分解的NaHCO3质量与加热前原NaHCO3质量的比值)。


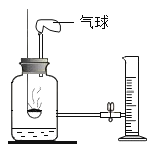
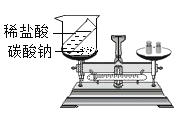 验证质量守恒定律 B.
验证质量守恒定律 B.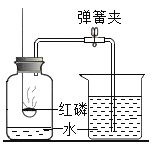 测定空气中氧气含量 C.
测定空气中氧气含量 C. 探究铁钉生锈的条件 D.
探究铁钉生锈的条件 D.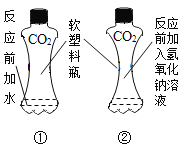 证明CO2与NaOH反应
证明CO2与NaOH反应