题目内容
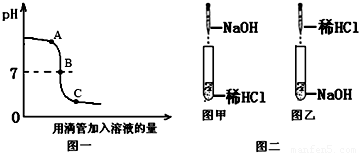
盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化如图一,请分析:(1)根据pH变化图象判断,该反应的实验过程是按照图二中的图______(填“甲”或“乙”)进行;
(2)图一中A、B、C 三点表示的溶液,二种反应物恰好完全反应的是______(填“A”、“B”或“C”,下同)点的溶液;此时溶液中一定含有的阳离子有______;
(3)为了证明盐酸与氢氧化钠溶液反应的生成物,小明的探究过程如下:
实验过程:向装有一定量稀盐酸的试管中滴加氢氧化钠溶液,振荡后再滴加硝酸银溶液.
观察现象:出现白色沉淀.
得出结论:证明生成了氯化钠.
小思认为该结论不正确.合理解释是______.
【答案】分析:(1)根据图象和和盐酸与氢氧化钠反应过程来分析;
(2)根据图象和和盐酸与氢氧化钠反应过程和物质的电离角度加以分析;
(3)利用稀盐酸与氢氧化钠溶液反应以及其产物与硝酸银溶液反应的知识加以判断.
解答:解:(1)从图象看随着物质的加入溶液的pH值越来越小,所以是往氢氧化钠溶液中加入稀盐酸.故答案为:乙.
(2)A、B、C 三点表示的溶液中,A时溶液显碱性,B时溶液显中性,C时溶液显酸性,溶液显中性时,酸碱恰好完全反应,显中性时溶液中的离子有钠离子、氯离子.故答案为:Na+.
(3)向装有一定量稀盐酸的试管中滴加氢氧化钠溶液时生成了氯化钠和水,当滴加硝酸银溶液时,生成了白色沉淀,但这白色沉淀不一定是氯化钠和硝酸银反应产生的,还有可能是当滴加氢氧化钠溶液不足时盐酸有剩余,剩余的稀盐酸与硝酸银溶液反应的产生的.故答案为:稀盐酸也会与硝酸银反应生成白色的氯化银沉淀.
点评:本题主要考察了中和反应的过程与图象的结合以及稀盐酸与氯化钠和硝酸银反应的相关知识,在做题时一定要注重反应的量的问题.
(2)根据图象和和盐酸与氢氧化钠反应过程和物质的电离角度加以分析;
(3)利用稀盐酸与氢氧化钠溶液反应以及其产物与硝酸银溶液反应的知识加以判断.
解答:解:(1)从图象看随着物质的加入溶液的pH值越来越小,所以是往氢氧化钠溶液中加入稀盐酸.故答案为:乙.
(2)A、B、C 三点表示的溶液中,A时溶液显碱性,B时溶液显中性,C时溶液显酸性,溶液显中性时,酸碱恰好完全反应,显中性时溶液中的离子有钠离子、氯离子.故答案为:Na+.
(3)向装有一定量稀盐酸的试管中滴加氢氧化钠溶液时生成了氯化钠和水,当滴加硝酸银溶液时,生成了白色沉淀,但这白色沉淀不一定是氯化钠和硝酸银反应产生的,还有可能是当滴加氢氧化钠溶液不足时盐酸有剩余,剩余的稀盐酸与硝酸银溶液反应的产生的.故答案为:稀盐酸也会与硝酸银反应生成白色的氯化银沉淀.
点评:本题主要考察了中和反应的过程与图象的结合以及稀盐酸与氯化钠和硝酸银反应的相关知识,在做题时一定要注重反应的量的问题.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
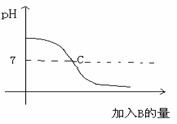
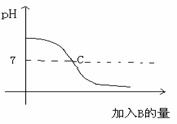
已知A、B分别是盐酸溶液和氢氧化钠溶液中的一种,右图表示向A中逐滴加入B时溶液的pH变化曲线。
请写出你从曲线中收获的信息。
(1)A是 溶液。 (2)C点表示的意义 是 。
(3)小红同学在验证氢氧化钠能否与稀盐酸反应时,操作如下图
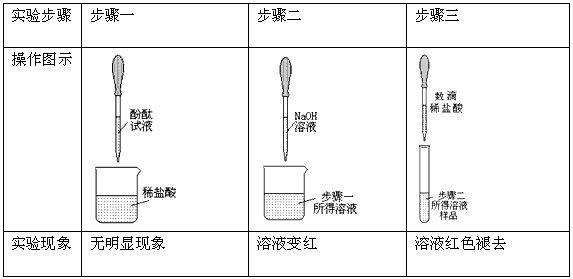
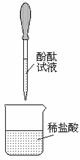
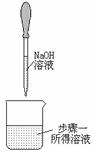
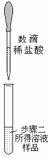
| 实验步骤 | 步骤一 | 步骤二 | 步骤三 |
| 操作图示 |
|
|
|
| 实验现象 | 无明显现象 | 溶液变红 | 溶液红色褪去 |
实验时小红发觉烧杯外壁发烫、溶液温度升高,小红联想到氢氧化钠固体溶于水溶液温度也升高,那么两实验温度升高的原理是否相同 ,理由是 。
 已知A、B分别是盐酸溶液和氢氧化钠溶液中的一种,
已知A、B分别是盐酸溶液和氢氧化钠溶液中的一种,
右图表示向A中逐滴加入B时溶液的pH变化曲线。
请写出你从曲线中收获的信息。
(1)A是 溶液。 (2)C点表示的意义 是 。
(3)小红同学在验证氢氧化钠能否与稀盐酸反应时,操作如下图
| 实验步骤 | 步骤一 | 步骤二 | 步骤三 |
| 操作图示 |
|
|
|
| 实验现象 | 无明显现象 | 溶液变红 | 溶液红色褪去 |
实验时小红发觉烧杯外壁发烫、溶液温度升高,小红联想到氢氧化钠固体溶于水溶液温度也升高,那么两实验温度升高的原理是否相同 ,理由是 。
已知A、B分别是盐酸溶液和氢氧化钠溶液中的一种,如图表示向A中逐滴加入B时溶液的pH变化曲线.
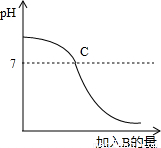
请写出你从曲线中收获的信息.
(1)A是 溶液.
(2)C点表示的意义 是 .
(3)小红同学在验证氢氧化钠能否与稀盐酸反应时,操作如图
实验时小红发觉烧杯外壁发烫、溶液温度升高,小红联想到氢氧化钠固体溶于水溶液温度也升高,那么两实验温度升高的原理是否相同 ,理由是 .

请写出你从曲线中收获的信息.
(1)A是 溶液.
(2)C点表示的意义 是 .
(3)小红同学在验证氢氧化钠能否与稀盐酸反应时,操作如图
| 实验步骤 | 步骤一 | 步骤二 | 步骤三 |
| 操作图示 | 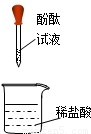 | 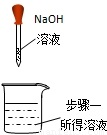 | 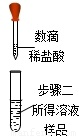 |
| 实验现象 | 无明显现象 | 溶液变红 | 溶液红色褪去 |