题目内容
铜和稀硝酸发生如下反应:3Cu+8HNO3═3Cu(NO3)2+2X↑+4H2O,其中X的化学式为( )
| A、N2O |
| B、N2 |
| C、NO |
| D、N2O2 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:化学反应前后,元素的种类不变,原子的种类、总个数不变.
解答:解:由3Cu+8HNO3═3Cu(NO3)2+2X↑+4H2O可知,
反应前铜原子是3个,反应后是3个;
反应前氢原子是8个,反应后氢原子是8个;
反应前氮原子是8个,反应后应该是8个,其中2个包含在2X中;
反应前氧原子是24个,反应后应该是24个,其中2个包含在2X中;
由分析可知,每个X中含有1个氮原子和1个氧原子,是一氧化氮,化学式是NO.
故选:C.
反应前铜原子是3个,反应后是3个;
反应前氢原子是8个,反应后氢原子是8个;
反应前氮原子是8个,反应后应该是8个,其中2个包含在2X中;
反应前氧原子是24个,反应后应该是24个,其中2个包含在2X中;
由分析可知,每个X中含有1个氮原子和1个氧原子,是一氧化氮,化学式是NO.
故选:C.
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
掌握好化学用语是学好化学的关键.下列化学用语与其含义相符的是( )
| A、O2--2个氧原子 | ||
| B、2N--2个氮元素 | ||
| C、SO2--二氧化硫 | ||
D、
|
下列化学用语既有宏观意义,又有微观意义的是( )
| A、H |
| B、2H+ |
| C、2H2 |
| D、2H |
下列有关Fe2O3的反应中,属于置换反应的是( )
| A、Fe2O3+6HCl=2FeCl3+3H2O | ||||
B、Fe2O3+3CO
| ||||
C、Fe2O3+3H2
| ||||
| D、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O |
虾青素(C40H52O4)是一种具有极强的抗肿瘤、抗氧化性能的物质,可增强动物免疫力.下列有关它的说法正确的是( )
| A、虾青素是一种氧化物 |
| B、虾青素是由96个原子构成 |
| C、虾青素的相对分子质量是596 |
| D、虾青素中碳、氢、氧元素的质量比是40:52:4 |
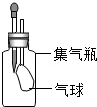 探究小组用右图装置进行实验.胶头滴管和集气瓶中分别盛装某种物质,挤压胶头滴管向集气瓶中滴加适量液体后,能观察到气球变大的组合是( )
探究小组用右图装置进行实验.胶头滴管和集气瓶中分别盛装某种物质,挤压胶头滴管向集气瓶中滴加适量液体后,能观察到气球变大的组合是( )| 组合 | 胶头滴管 | 集气瓶 |
| A | 稀盐酸 | Na2CO3 |
| B | 稀硫酸 | Zn |
| C | 澄清石灰水 | 二氧化碳 |
| D | 水 | 生石灰CaO |
| A、A | B、B | C、C | D、D |
日常生活中所见到的“加碘食盐”、“含氟牙膏”、“高钙牛奶”、“补铁酱油”中的“碘、氟、钙、铁”应理解为( )
| A、原子 | B、单质 | C、分子 | D、元素 |