题目内容
 水是人类生活中不可缺少的物质.
水是人类生活中不可缺少的物质.(1)下列净水方法中,通常用于除去水中难溶性杂质的是
A
A
,净水程度最高的是C
C
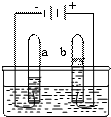
. A.过滤 B.煮沸 C.蒸馏 D.吸附(2)如图为电解水的装置.用
带火星的木条
带火星的木条
来检验b管中的气体.b管中 气体与a管中气体的质量比为8:1
8:1
.反应的化学方程式为2H2O
2H2↑+O2↑
| ||
2H2O
2H2↑+O2↑
,由实验得出水是由
| ||
氢、氧两种元素
氢、氧两种元素
组成的.(3)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一.请写出Ca(HCO3)2受热分解的化学方程式:
Ca(HCO3)2
CaCO3↓+H2O+CO2↑
| ||
Ca(HCO3)2
CaCO3↓+H2O+CO2↑
.
| ||
分析:(1)过滤是将不溶性固体从液体中分离出来的操作方法;蒸馏是将水气化后冷凝的方法,此时得到的水称为蒸馏水,是纯净的水;
(2)水通电分解时,与正极相连的试管内得到氧气,与负极相连的试管内得到氢气,两种气体质量比为8:1;由此实验可证明水由氢、氧两种元素组成;
(3)根据题中信息可知:碳酸氢钙受热分解可生成碳酸钙、水和二氧化碳,完成反应化学方程式.
(2)水通电分解时,与正极相连的试管内得到氧气,与负极相连的试管内得到氢气,两种气体质量比为8:1;由此实验可证明水由氢、氧两种元素组成;
(3)根据题中信息可知:碳酸氢钙受热分解可生成碳酸钙、水和二氧化碳,完成反应化学方程式.
解答:解:(1)除去水中难溶性杂质需要进行过滤操作;蒸馏处理后的水为蒸馏水,是纯净的水,因此蒸馏是净水程度最高的方法;
(2)如题图所示,b管与电源正极相连,该管内得到的为氧气,电解水时所得到氧气与氢气的质量比与水中氧、氢元素质量比相同,为8:1;反应的化学方程式为2H2O
2H2↑+O2↑;分解得到的氢气、氧气分别由氢元素、氧元素组成,因此可推断水是由氢、氧两种元素组成;
(3)Ca(HCO3)2受热分解生成碳酸钙、水和二氧化碳,反应的化学方程式为Ca(HCO3)2
CaCO3↓+H2O+CO2↑.
故答案为:
(1)A;C;
(2)带火星的木条;8:1;2H2O
2H2↑+O2↑;氢、氧两种元素;
(3)Ca(HCO3)2
CaCO3↓+H2O+CO2↑.
(2)如题图所示,b管与电源正极相连,该管内得到的为氧气,电解水时所得到氧气与氢气的质量比与水中氧、氢元素质量比相同,为8:1;反应的化学方程式为2H2O
| ||
(3)Ca(HCO3)2受热分解生成碳酸钙、水和二氧化碳,反应的化学方程式为Ca(HCO3)2
| ||
故答案为:
(1)A;C;
(2)带火星的木条;8:1;2H2O
| ||
(3)Ca(HCO3)2
| ||
点评:本题综合考查水的净化、水的电解及化学方程式的书写,解答时应逐一分析,切勿混为一谈.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目