题目内容
【题目】某兴趣小组对“水的化学式是如何以实验方法确定的”进行研究.【提出假设】设水的化学式为H2O;
【查阅资料】在标准状况下,氢气的密度ρ(H2)=0.09g/L,氧气的密度ρ(O2)=1.43g/L,氢的相对原子质量为l,氧的相对原子质量为16;
【研究原理】运用化合物中各元素的质量之比等于组成该化合物各元素的实际质量之比的原理,求出一个水分子中氢原子和氧原子的个数之比;
(1)【实验探究】
实验操作 | 实验装置图 | 实验记录及结果 |
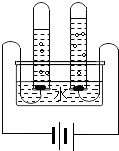
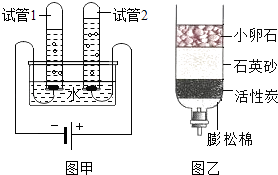
①用如图所示的装置电解水 |
| ①经检验,负极产生的气体是 , 正极产生的气体是 . |
(2)【数据处理】兴趣小组首先设水的化学式为HxOy,再根据实验结果及有关数据,并利用研究原理进行了计算.请你将其计算过程进行补充.(最后结果取整数)【得出结论】兴趣小组提出的假设 . (填“正确”或”不正确”)
【答案】
(1)氢气;氧气;2:1
(2)正确
【解析】解:【实验探究】电解水实验的现象是电极上出现气泡,负极是氢气,正极是氧气,两者的体积比为2:1;说明:水是由氢、氧两元素组成的.
【数据处理】根据生成的氢气与氧气的体积比是2:1,根据m=ρv,可知氢气和氧气的质量比是: ![]() =
= ![]() ;根据各元素的质量比=各元素相对原子质量×相应原子个数乘积之比,水中氢、氧元素质量比为(1×x):(16×y)=x:16y=1:8,可得:x:y=1:2;
;根据各元素的质量比=各元素相对原子质量×相应原子个数乘积之比,水中氢、氧元素质量比为(1×x):(16×y)=x:16y=1:8,可得:x:y=1:2;
【得出结论】有计算可知化学式为:H2O.
所以答案是:【实验探究】氢气;氧气;2:1;
【数据处理】氢气和氧气的质量比是: ![]() =
= ![]() ;水中氢、氧元素质量比为(1×x):(16×y)=x:16y=1:8,可得:x:y=2:1;
;水中氢、氧元素质量比为(1×x):(16×y)=x:16y=1:8,可得:x:y=2:1;
【得出结论】正确;
【考点精析】本题主要考查了电解水实验的相关知识点,需要掌握电解水的实验:A.装置―――水电解器B.电源种类---直流电C.加入硫酸或氢氧化钠的目的----增强水的导电性D.化学反应:2H2O=== 2H2↑+ O2↑才能正确解答此题.