题目内容
某化学兴趣小组通过课内和课外学习了有关氧气的知识:
(1)工业上主要用分离液态空气的方法制氧气,所利用的原理是
也可对水进行通电得到氧气,该反应用化学式可以表示为
这两种方法相比较而言
(2)实验室中可以用氯酸钾或双氧水制取氧气.用化学式表示这两个反应
①
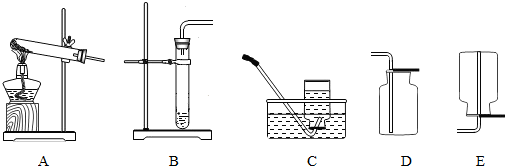
(3)兴趣小组的同学为了研究氧气的化学性质,现在准备用氯酸钾和二氧化锰的混合物制取氧气,并完成铁丝燃烧的实验,

a.他们所选的制取氧气的发生装置为(填序号,下同)
b.若要使收集到的氧气比较纯净(不含氮气),最好选用
c.正确的实验步骤为(填序号)
①熄灭酒精灯 ②从水槽中取出导管 ③用排水法收集气体 ④点燃酒精灯
⑤从下至上,从左至右连接仪器 ⑥装药品 ⑦检查装置的气密性
d.通过实验他们发现铁丝在纯氧中能够燃烧,用化学方程式表示该反应:
实验结束后,他们发现集气瓶底部被炸裂而出现了一道裂痕,请你帮助他们分析原因:
(1)工业上主要用分离液态空气的方法制氧气,所利用的原理是
氮气和氧气的沸点不同
氮气和氧气的沸点不同
.也可对水进行通电得到氧气,该反应用化学式可以表示为
2H2O
2H2↑+O2↑
| ||
2H2O
2H2↑+O2↑
.
| ||
这两种方法相比较而言
后
后
者(填”前”或”后”)耗能较多,前者的变化是物理
物理
变化(填”物理”或”化学”).(2)实验室中可以用氯酸钾或双氧水制取氧气.用化学式表示这两个反应
①
2KClO3
2KCl+3O2 ↑
| ||
| △ |
2KClO3
2KCl+3O2 ↑
②
| ||
| △ |
2H2O2
2H2O+O2 ↑
| ||
2H2O2
2H2O+O2 ↑
| ||
(3)兴趣小组的同学为了研究氧气的化学性质,现在准备用氯酸钾和二氧化锰的混合物制取氧气,并完成铁丝燃烧的实验,

a.他们所选的制取氧气的发生装置为(填序号,下同)
A
A
;b.若要使收集到的氧气比较纯净(不含氮气),最好选用
C
C
;c.正确的实验步骤为(填序号)
⑤⑦⑥④③②①
⑤⑦⑥④③②①
①熄灭酒精灯 ②从水槽中取出导管 ③用排水法收集气体 ④点燃酒精灯
⑤从下至上,从左至右连接仪器 ⑥装药品 ⑦检查装置的气密性
d.通过实验他们发现铁丝在纯氧中能够燃烧,用化学方程式表示该反应:
3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
现象是:
| ||
剧烈燃烧,火星四射,放出热量,生成黑色固体
剧烈燃烧,火星四射,放出热量,生成黑色固体
.实验结束后,他们发现集气瓶底部被炸裂而出现了一道裂痕,请你帮助他们分析原因:
集气瓶的底部没有放少量水或细沙
集气瓶的底部没有放少量水或细沙
.分析:(1)工业上主要用分离液态空气的方法制取氧气,是利用了氮气和氧气的沸点不同;水通电生成氢气和氧气,据此书写方程式;然后依据两种制取氧气的方法进行分析解答;
(2)根据氯酸钾和双氧水制取氧气的反应原理书写方程式;
(3)a、用高锰酸钾制取氧气的装置为“固体加热型”,据此进行选择;
b、若要使收集到的氧气比较纯净,应用排水法收集;
c、根据加热分解高锰酸钾制氧气的实验步骤:连→查→装→定→点→收→移→熄,进行解答;
d、根据铁丝在纯氧中燃烧的反应原理书写化学方程式;并根据铁丝在氧气中燃烧的现象和注意事项分析解题.
(2)根据氯酸钾和双氧水制取氧气的反应原理书写方程式;
(3)a、用高锰酸钾制取氧气的装置为“固体加热型”,据此进行选择;
b、若要使收集到的氧气比较纯净,应用排水法收集;
c、根据加热分解高锰酸钾制氧气的实验步骤:连→查→装→定→点→收→移→熄,进行解答;
d、根据铁丝在纯氧中燃烧的反应原理书写化学方程式;并根据铁丝在氧气中燃烧的现象和注意事项分析解题.
解答:解:(1)工业上使用分离液态空气的方法制取氧气,是利用了氮气的沸点比氧气的沸点低,从而将氧气分离出来;水在通电的情况下生成氢气和氧气,相比较而言电解水要消耗电能,耗能较多;分离液态空气过程中无新物质生成,故属于物理变化;
故答案为:氮气和氧气的沸点不同; 2H2O
2H2↑+O2↑; 后; 物理.
(2)氯酸钾在加热、二氧化锰作催化剂的条件下生成氯化钾和氧气,双氧水在二氧化锰的催化作用下分解生成水和氧气;
故答案为:2KClO3
2KCl+3O2 ↑;2H2O2
2H2O+O2 ↑(方程式不分先后);
(3)a、用高锰酸钾制取氧气的装置为“固体加热型”,所以选择发生装置A;
b、若要使收集到的氧气比较纯净,应用排水法收集;
c、根据加热分解高锰酸钾制氧气的实验步骤:连→查→装→定→点→收→移→熄,可知正确的实验步骤为:⑤⑦⑥④③②①;
d、铁丝在纯氧中燃烧生成四氧化三铁;反应时放出热量,剧烈燃烧、火星四射,生成黑色固体;在实验时要在集气瓶底预先铺上一层细沙或少量的水,防止生成的高温熔融物落下来炸裂集气瓶;
故答案为:
a.A;
b.C;
c.⑦⑥⑤④③②①;
d.3Fe+2O2
Fe3O4;剧烈燃烧,火星四射,放出热量,生成黑色固体; 集气瓶的底部没有放少量水或细沙.
故答案为:氮气和氧气的沸点不同; 2H2O
| ||
(2)氯酸钾在加热、二氧化锰作催化剂的条件下生成氯化钾和氧气,双氧水在二氧化锰的催化作用下分解生成水和氧气;
故答案为:2KClO3
| ||
| △ |
| ||
(3)a、用高锰酸钾制取氧气的装置为“固体加热型”,所以选择发生装置A;
b、若要使收集到的氧气比较纯净,应用排水法收集;
c、根据加热分解高锰酸钾制氧气的实验步骤:连→查→装→定→点→收→移→熄,可知正确的实验步骤为:⑤⑦⑥④③②①;
d、铁丝在纯氧中燃烧生成四氧化三铁;反应时放出热量,剧烈燃烧、火星四射,生成黑色固体;在实验时要在集气瓶底预先铺上一层细沙或少量的水,防止生成的高温熔融物落下来炸裂集气瓶;
故答案为:
a.A;
b.C;
c.⑦⑥⑤④③②①;
d.3Fe+2O2
| ||
点评:本题较综合的考查了氧气的工业和实验室制法的相关知识,及铁丝燃烧实验的相关内容,能很好的考查出学生对知识的掌握和应用.

练习册系列答案
 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
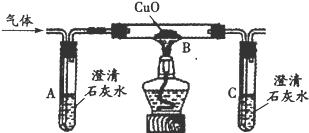
 某校化学课外兴趣小组的同学在研究性学习课上展示了一套如下图所示实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:H2C2O4
某校化学课外兴趣小组的同学在研究性学习课上展示了一套如下图所示实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:H2C2O4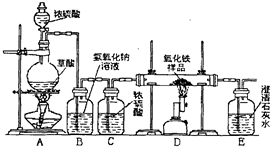 某校化学课外兴趣小组的同学在研究性学习课展示了一套如图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:
某校化学课外兴趣小组的同学在研究性学习课展示了一套如图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应: