题目内容
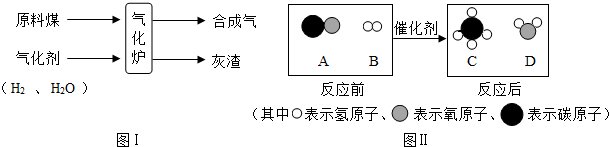
在反应A+B═C+D中,反应物的质量比m(A):m(B)=5:2.若完全反应后生成C和D共2.1g,则消耗反应物A为 g,B为 g.
【答案】分析:依据质量守恒定律中反应物质量总和等于反应后生成物的质量总和,所以依据C和D的质量和可知A和B的质量和,而后依据A和B的质量之比可求出参加反应的A和B的质量;
解答:解:依据质量守恒定律中反应物质量总和等于反应后生成物的质量总和,所以依据C和D的质量和可知A和B的质量和也为2.1g,由于反应物的质量比m(A):m(B)=5:2,即5份质量的A恰好和2份质量的B反应,所以参加反应的B的质量是2.1g× =0.6g,A的质量为2.1g×
=0.6g,A的质量为2.1g× =1.5g;
=1.5g;
故答案为:1.5;0.6;
点评:在化学反应中遵循质量守恒定律,参加反应的物质的质量总和等于反应后生成的物质的质量总和是解题的关键;
解答:解:依据质量守恒定律中反应物质量总和等于反应后生成物的质量总和,所以依据C和D的质量和可知A和B的质量和也为2.1g,由于反应物的质量比m(A):m(B)=5:2,即5份质量的A恰好和2份质量的B反应,所以参加反应的B的质量是2.1g×
 =0.6g,A的质量为2.1g×
=0.6g,A的质量为2.1g× =1.5g;
=1.5g;故答案为:1.5;0.6;
点评:在化学反应中遵循质量守恒定律,参加反应的物质的质量总和等于反应后生成的物质的质量总和是解题的关键;

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目