题目内容
(2013?常州)某肉联厂在鲜肉表面涂抹白色粉末A以延长保持时间.小新进行了如下实验,探究化合物A的化学组成.
【定性研究】
根据上述实验可初步推知,A是
【定量研究】
为进一步探究A的化学组成,进行如下实验:
①将盛有292g质量分数为12.5%的稀盐酸的装置置于电子天平上(该装置可确保氯化氢和水蒸气不逸出);
②向装置中加入2.0gA,在天平读数不再变化时记录数据;
③重复②若干次;
④以mA(加入A的质量)为横坐标、以△m(溶液的增重)为纵坐标,绘得下图.
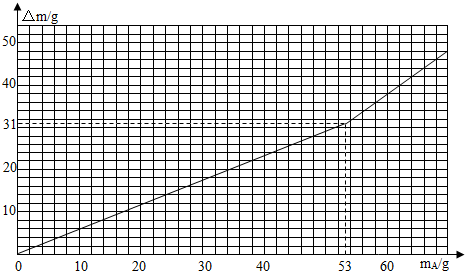
通过计算回答下列问题:
(1)实验中反应生成的气体的总质量为
(2)A中阳离子与阴离子质量的最简整数比为
(3)A的化学式为
【定性研究】
| 步骤 | 实验操作 | 实验现象 |
| ① | 取样于试管中,加足量蒸馏水,振荡 | 样品消失,得到无色澄清溶液 |
| ② | 向步骤①所得溶液中滴加无色酚酞试液 | 溶液变红 |
| ③ | 向步骤②所得溶液中滴加稀盐酸至过量 | 产生无色、无气温的气体,溶液褪色 |
碳酸盐
碳酸盐
;【定量研究】
为进一步探究A的化学组成,进行如下实验:
①将盛有292g质量分数为12.5%的稀盐酸的装置置于电子天平上(该装置可确保氯化氢和水蒸气不逸出);
②向装置中加入2.0gA,在天平读数不再变化时记录数据;
③重复②若干次;
④以mA(加入A的质量)为横坐标、以△m(溶液的增重)为纵坐标,绘得下图.

通过计算回答下列问题:
(1)实验中反应生成的气体的总质量为
22
22
g;(2)A中阳离子与阴离子质量的最简整数比为
23:30
23:30
;(3)A的化学式为
Na2CO3
Na2CO3
.分析:【定性研究】
根据物质的水溶性、溶液酸碱性、与稀盐酸相互作用的情况可以判断物质;
【定量研究】
(1)通过实验数据可以计算生成气体的质量;
(2)根据物质的化学式可以计算离子之间的质量比;
(3)物质的名称和化学式是相对应的.
根据物质的水溶性、溶液酸碱性、与稀盐酸相互作用的情况可以判断物质;
【定量研究】
(1)通过实验数据可以计算生成气体的质量;
(2)根据物质的化学式可以计算离子之间的质量比;
(3)物质的名称和化学式是相对应的.
解答:解:白色粉末溶于水得到的溶液能使酚酞试液变红色,说明溶液显碱性;
滴加过量的稀盐酸能生成无色、无味的气体、溶液褪色,说明白色粉末中含有碳酸根,属于碳酸盐;
由图象数据“加入53g白色粉末时与292g12.5%的稀盐酸恰好完全反应、溶液增重31g”可知逸出气体的质量为:53g-31g=22g,
292g12.5%的稀盐酸中溶质氯化氢的质量为:292g×12.5%=36.5g,
由Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 44
53g 36.5g 22g
可知,可溶性物质是碳酸钠.
【定性研究】
根据上述实验可初步推知,A是碳酸盐.
故填:碳酸盐.
【定量研究】
(1)实验中反应生成的气体的总质量为22g.
故填:22.
(2)A中阳离子与阴离子质量的最简整数比为:46:60=23:30.
故填:23:30.
(3)A的化学式为:Na2CO3.
故填:Na2CO3.
滴加过量的稀盐酸能生成无色、无味的气体、溶液褪色,说明白色粉末中含有碳酸根,属于碳酸盐;
由图象数据“加入53g白色粉末时与292g12.5%的稀盐酸恰好完全反应、溶液增重31g”可知逸出气体的质量为:53g-31g=22g,
292g12.5%的稀盐酸中溶质氯化氢的质量为:292g×12.5%=36.5g,
由Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 44
53g 36.5g 22g
可知,可溶性物质是碳酸钠.
【定性研究】
根据上述实验可初步推知,A是碳酸盐.
故填:碳酸盐.
【定量研究】
(1)实验中反应生成的气体的总质量为22g.
故填:22.
(2)A中阳离子与阴离子质量的最简整数比为:46:60=23:30.
故填:23:30.
(3)A的化学式为:Na2CO3.
故填:Na2CO3.
点评:碳酸钠、碳酸氢钠都是可溶性碳酸盐,与稀盐酸反应都能够生成二氧化碳,本题中只有通过计算才能确定碳酸盐的类型.

练习册系列答案
相关题目
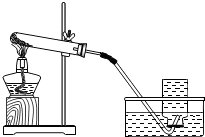 (2013?常州)使用如图所示装置制取氧气.
(2013?常州)使用如图所示装置制取氧气.