题目内容
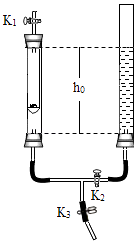
【题目】利用下图装置进行实验(两支玻璃管内径相同).实验前K1、K2、K3均已关闭.
实验装置 | 【实验1】制备气体 | 【实验2】测定空气中氧气含量 |
| 左管中带孔的燃烧匙盛有足量锌粒,右管盛有稀硫酸 | 左管中燃烧匙盛有足量白磷,右管盛有水 |
(1)实验1:锌与稀硫酸反应的化学方程式为;为使反应停止,Ⅲ中的操作是 .
(2)实验2:打开K2 , 右管中液面下降,原因是;计算空气中氧气体积分数的表达式为(用h0、h1表示).
【答案】
(1)Zn+H2SO4=ZnSO4+H2↑;关闭K1
(2)左侧玻璃管内白磷燃烧消耗氧气,压强减小;![]() ×100%
×100%
【解析】解:(1)锌与稀硫酸反应生成硫酸锌和氢气,化学方程式为:Zn+H2SO4=ZnSO4+H2↑;为使反应停止,关闭K1 , 左管中产生的氢气无法排除,管内压强变大,将稀硫酸压回到右管中,锌与稀硫酸分离,反应停止;(2)左侧玻璃管内白磷燃烧消耗氧气,使右侧管中压强变小,打开K2 , 右侧水进入左侧管中,右管中液面下降;被吸入左侧的水即为消耗氧气的体积,假设管的横截面积为s,所以最终测得的空气中氧气体积分数为 ![]() =
= ![]() ×100%. 所以答案是:(1)Zn+H2SO4=ZnSO4+H2↑;关闭K1;(2)左侧玻璃管内白磷燃烧消耗氧气,压强减小;
×100%. 所以答案是:(1)Zn+H2SO4=ZnSO4+H2↑;关闭K1;(2)左侧玻璃管内白磷燃烧消耗氧气,压强减小; ![]() ×100%.
×100%.
【考点精析】根据题目的已知条件,利用金属材料的选择依据和书写化学方程式、文字表达式、电离方程式的相关知识可以得到问题的答案,需要掌握黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属;注意:a、配平 b、条件 c、箭号.

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案