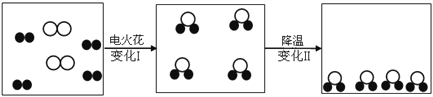
题目内容
【题目】已知氯化钠、碳酸钠在不同温度时的溶解度如下:
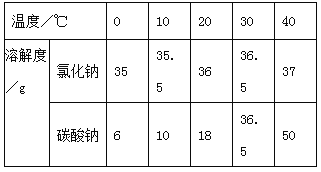
⑴依据上表数据,绘制出了氯化钠和碳酸钠的溶解度曲线(如下图),图中能表示碳酸钠
溶解度曲线的是________(填“A”或“B”)。
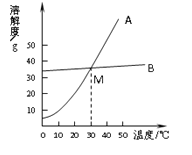
⑵图中两溶解度曲线相交于M点,此点表示的意义是____________________________。
⑶40℃时,把50 g A物质放入100 g水中,充分搅拌,所得溶液是________________溶液(填“饱和”或“不饱和”)。
【答案】 A 30℃时,NaCl和Na2CO3的溶解度相同 饱和
【解析】本题考查了主要考查了固体溶解度曲线的意义及根据固体的溶解度曲线解决相关的问题。(1)依据上表数据可知,碳酸钠溶解度受温度变化影响较大,因此图中能表示碳酸钠溶解度曲线的是A;
(2)图中两溶解度曲线相交于M点,此点是30℃时,A和B的溶解度曲线的交点,表示30℃时,NaCl和Na2CO3的溶解度相同;
(3)A是碳酸钠的溶解度曲线,由表中数据可知:40℃时,碳酸钠的溶解度是50g,即100g水中最多溶解50g碳酸钠恰好饱和,所以把50gA物质放入100g水中,充分搅拌,所得溶液是饱和溶液。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】用下列装置对碳及其氧化物的性质进行系列实验探究。

实验 | 物质 | 问 题 | |
X | Y | ||
实验一 | CO | CuO | (1)实验开始前先通CO一段时间赶尽装置内空气。通过________________现象,可知装置内充满了CO气体。 (2)写出A处反应的化学方程式_________________,其中氧化铜发生_________(选填“氧化”或“还原”)反应。 (3)C中实验现象__________________。 (4)该实验能证明CO的化学性质是___________。 |
实验二 | CO2 | C | 写出A处反应的化学方程式________________,通过__________________现象,能证明该反应发生。 (2)B装置的作用是_______________。 (3)若2molC完全反应完,需要消耗________CO2。 I.1mol II. 2mol III. >2mol IV.无法判断 |
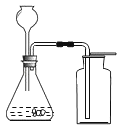
【题目】某校实验小组取酸性锌锰干电池进行探究,他们发现电池内部结构如图1所示。
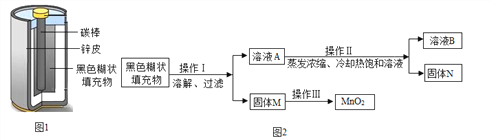
【查阅资料】
⑴锌皮为金属锌(含有少量的铁)
⑵黑色糊状填充物由炭黑、MnO2、ZnC12和NH4Cl等组成
⑶有关数据见下表
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 | |
【实验探究一】小明取适量黑色糊状填充物,按图2所示实验流程进行探究。
⑴溶液A中溶质主要有ZnC12和NH4Cl,操作Ⅱ中采用冷却热饱和溶液的方法实现两者分离的依据是______________________;
⑵欲从固体M 中得到较纯的MnO2,操作Ⅲ可采用的简便方法是_________。
【实验探究二】小明取电池外壳锌皮,用砂纸打磨干净,剪成小块,进行实验。
⑴取一块锌皮放入盛有适量稀盐酸的烧杯中, 实验中可观察到的现象是_____________有关反应的化学方程式___________________________。
⑵下列各组物质混合后,也能生成ZnCl2的有_______(填字母序号)。
A. ZnO与稀盐酸 B. Zn与NaCl溶液 C. Zn(NO3)2溶液与NH4Cl溶液
【题目】实验研究是化学学习的重要方法。请以碳及其化合物的知识进行以下实验研究。
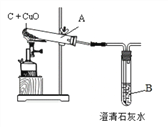
实验一:木炭还原氧化铜。
①观察到B中溶液变浑浊,试管A中的现象_______________,
A中反应的化学方程式为________,还原剂是__________。
②反应完全后,若先撤走酒精喷灯停止加热,可能导致的后果___________________________
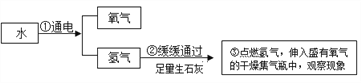
实验二:为了探究某混合气体是由水蒸气、一氧化碳、二氧化碳3种气体组成, 设计了如下实验:
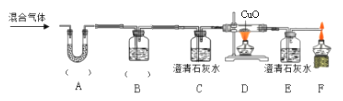
①欲探究混合气体中含有CO2和H2O蒸气,在图中的A、B装置内依次盛放的化学试剂为_______;检验出水蒸气的现象是_____________,反应的化学方程式为__________。
②装置E、F的作用分别是__________________ 、_____________________,E中反应的化学方程式为_____________。
③若没有装置E_______________(填“能”或“否”)证明混合气体中含有一氧化碳,请简述理由_____________________。
④实验结束后先熄灭装置D处的酒精灯,E中石灰水不会倒流的原因是____________。
⑤该实验中体现的一氧化碳的化学性质有__________________________。
实验三:有些化妆品中添加的高纯度碳酸钙可以用石灰石来制备,如下图。(假设石灰石中除碳酸钙外。所含杂质仅为SiO2,其不溶于水,高温不会分解,也不与盐酸反应)
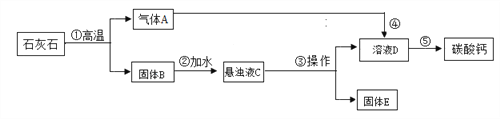
Ⅰ. 写出步骤①②中反应的化学方程式____________、____________。
Ⅱ. 气体A能使紫色石蕊试液变红色,反应的化学方程式为____________ 。
Ⅲ. 操作⑤的目的是________,用到的仪器主要有玻璃棒、酒精灯、铁架台(带铁圈)、__________。
Ⅳ. 为验证实验结束后得到的固体B中碳酸钙是否已经完全分解,请设计两种方案完成下表内容。
实验步骤 | 实验现象 | 结论 | |
方案一(66) | ________________ | ________________ | ________________ |
方案二(67) | ________________ | ________________ | ________________ |
【题目】某中学化学课外兴趣小组的同学为了寻找新的催化剂,设计了如下探究方案。
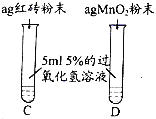
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】
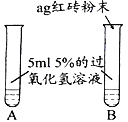
实验步骤 | 实验现象 | 实验结论及解释 |
Ⅰ. | A中无明显现象, B中产生大量能使带火星木条复燃的气体 | ① 产生的气体是___ ② 红砖粉末能改变过氧化氢分解速率 |
Ⅱ. 向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ① 又产生大量能使带火星木条复燃的气体 ② 滤渣质量等于ag | 红砖粉末的________和____________在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
Ⅲ. | 两试管中均产生气泡,但____(填“C”或“D”)试管中产生的气泡快。 | 红砖粉末的催化效果没有二氧化锰粉末好 |