题目内容
【题目】化学实验是科学探究的重要途径。
(1)在实验室,浓硫酸要密封保存的原因是______。(填字母代号)
a.防潮解 b.防挥发 c.防氧化 d.防吸水
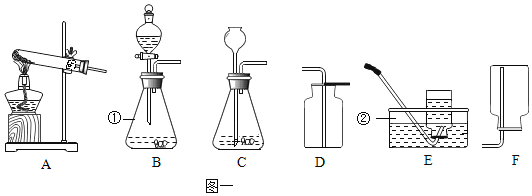
(2)探究小组的同学设计如图所示的微型实验装置来探究二氧化碳的制法和性质,打开弹簧夹,并推压加液器的活塞加入盐酸。
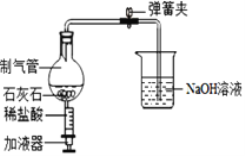
①写出制气管中发生反应的化学方程式______
②当制气管中盐酸消耗完,反应停止一段时间后,可观察到什么现象______?
③该制气管具有控制反应开始与结束的优点,利用该优点,还可以制取其他气体, 写出其反应方程式______。
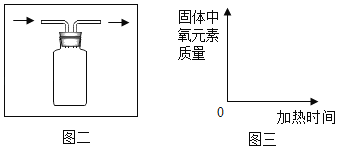
(3)探究小组的同学利用下图装置做CO还原CuO的实验,并检验气体产物,已知混合气体中还含有CO2和H2O。
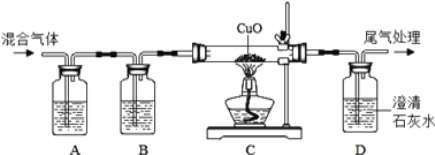
①A、B装置中应分别盛放什么试剂______?
②装置C中可观察到什么实验现象______?
③CO2制取的发生装置与氢气相同,请在方框中画出CO2发生装置图______(只画试管和导气管)

(4)向一定量的碳酸钠粉末中加入100g的稀盐酸,反应一段时间后,固体全部溶解,溶液的质量增加到了106.2g,求碳酸钠粉末的质量______。
【答案】d CaCO3+2HCl=CaCl2+H2O+CO2↑ 烧杯中的水沿导管倒吸进入制气管且液体中有白色沉淀产生 Zn+H2SO4=ZnSO4+H2↑ 氢氧化钠溶液浓硫酸溶液 固体由黑色变红色 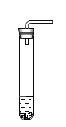 10.6g
10.6g
【解析】
(1)浓硫酸具有吸水性,在实验室中要密封保存,故选d;
(2)①石灰石和稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
②当制气管中盐酸消耗完,反应停止后,二氧化碳和氢氧化钠反应而消耗,使装置内的压强降低,烧杯中的水沿导管进入制气管,碳酸钙和稀盐酸反应生成的氯化钙,钙离子反应生成的二氧化碳反应生成碳酸钙白色沉淀;
③该制气管具有控制反应开始与结束的优点,利用该优点,还可以利用锌粒和稀盐酸反应制取氢气,反应方程式:Zn+H2SO4=ZnSO4+H2↑。
(3)①要先除去二氧化碳,再用浓硫酸除去水,所以,A中放氢氧化钠溶液,B中浓硫酸溶液;
②若原混合气体中含有CO,一氧化碳和氧化铜在高温下反应生成铜和二氧化碳,故可观察到C中黑色粉末变成红色,D中澄清石灰水变浑浊;
③实验室制取二氧化碳为大理石和稀盐酸反应,固液常温发生装置,制取氢气为锌和稀盐酸反应,固液常温型发生装置,故CO2制取的发生装置如图所示: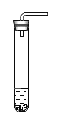 ;
;
(4)解:设碳酸钠粉末的质量为x。

![]()
解得:x=10.6g
答:碳酸钠粉末的质量为10.6g。