题目内容
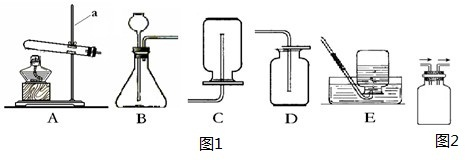
气体的实验室制取是初中非常重要的一组实验,结合下列图1实验装置回答有关问题:
(1)仪器a的名称是______.
(2)在初中可同时用来制取O2、CO2和H2的发生装置是______填字母).
(3)请写出检查装置A气密性是否良好的方法______ 用高锰酸钾制取O2,装置A还需做的一点小改动是______.
(4)实验室常用亚硫酸钠(Na2SO3)固体与浓硫酸反应生成硫酸钠、水和二氧化硫来制取SO2.
已知:SO2是一种没有颜色而有刺激性气味的有毒气体,易溶于水,密度比空气大,常温下在空气中不反应.
①制取SO2的化学方程式为______.
②在收集SO2,为了避免SO2对环境的污染,对SO2的收集装置作了改进(见图2),请你把集气瓶内的导管补充完整(图中“→”表示气体流向).
解:(1)根据教材中实验室常用仪器可知a为铁架台;
(2)制氧气可以用双氧水和二氧化锰,制二氧化碳可以用碳酸钙和稀盐酸,制氢气可以用稀硫酸和锌粒,都是固体和液体反应,条件不需要加热,所以发生装置可用B;
(3)检查装置A气密性的方法:把导气管的一端插入水中,双手握住试管,看到导管口有气泡冒出,说明装置气密性良好;用高锰酸钾制取O2,装置A还需做的一点小改动是在试管口处塞一团棉花,以防止高锰酸钾粉末进入导管;
(4)①实验室常用亚硫酸钠(Na2SO3)固体与浓硫酸常温下反应来制取SO2,化学方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;②因为SO2是一种没有颜色而有刺激性气味的有毒气体,易溶于水,密度比空气大,常温下在空气中不反应,故可用向上排空气法收集,收集装置改进为: .
.
故答案为:(1)铁架台;(2)B;(3)把导气管的一端插入水中,双手握住试管,看到导管口有气泡冒出,说明装置气密性良好.;在试管口处塞一团棉花;(4)①Na2SO3+H2SO4=Na2SO4+SO2+H2O↑;②
分析:(1)根据教材中实验室常用仪器判断;
(2)根据药品的状态和反应所需的条件选择发生装置;根据气体的性质如溶解性,密度,是否与空气中的成分或水发生反应来确定收集装置;
(3)根据检查装置A气密性的方法分析;根据用高锰酸钾制取O2的注意事项;
(4)根据SO2制取时药品的状态和反应所需的条件选择发生装置,根据气体的性质如溶解性,密度,是否与空气中的成分或水发生反应来确定收集装置.
点评:化学是一门以实验为基础的学科,因此实验仪器的使用,装置的选择,实验原理,注意事项,气体的检验,都是考试热点.
(2)制氧气可以用双氧水和二氧化锰,制二氧化碳可以用碳酸钙和稀盐酸,制氢气可以用稀硫酸和锌粒,都是固体和液体反应,条件不需要加热,所以发生装置可用B;
(3)检查装置A气密性的方法:把导气管的一端插入水中,双手握住试管,看到导管口有气泡冒出,说明装置气密性良好;用高锰酸钾制取O2,装置A还需做的一点小改动是在试管口处塞一团棉花,以防止高锰酸钾粉末进入导管;
(4)①实验室常用亚硫酸钠(Na2SO3)固体与浓硫酸常温下反应来制取SO2,化学方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;②因为SO2是一种没有颜色而有刺激性气味的有毒气体,易溶于水,密度比空气大,常温下在空气中不反应,故可用向上排空气法收集,收集装置改进为:
 .
.故答案为:(1)铁架台;(2)B;(3)把导气管的一端插入水中,双手握住试管,看到导管口有气泡冒出,说明装置气密性良好.;在试管口处塞一团棉花;(4)①Na2SO3+H2SO4=Na2SO4+SO2+H2O↑;②

分析:(1)根据教材中实验室常用仪器判断;
(2)根据药品的状态和反应所需的条件选择发生装置;根据气体的性质如溶解性,密度,是否与空气中的成分或水发生反应来确定收集装置;
(3)根据检查装置A气密性的方法分析;根据用高锰酸钾制取O2的注意事项;
(4)根据SO2制取时药品的状态和反应所需的条件选择发生装置,根据气体的性质如溶解性,密度,是否与空气中的成分或水发生反应来确定收集装置.
点评:化学是一门以实验为基础的学科,因此实验仪器的使用,装置的选择,实验原理,注意事项,气体的检验,都是考试热点.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案
相关题目
(1)实验室给你提供了下列仪器,请选用合适的仪器完成指定的实验

①要制取较多的O2用来探究其性质(要求制取过程中可以添加反应物),组装气体发生装置需要的仪器是 ![]() (填序号),收集氧气应采用 向上排空气 法。
(填序号),收集氧气应采用 向上排空气 法。
②提纯初盐时,过滤需要选用上述仪器中的 (填序号),出此之外还缺少的仪器是滤纸、 、 (填名称)。
(2)美羊羊同学的购物袋装薯片中发现还有一个小袋,上面![]() 标有“成分:CaO、Fe;作用:防潮、防氧化;警告:禁止食用”等字样,撕开小袋,发现里面的固体粉末有少许是棕红色,大多数是灰白色的。经过分析,她认为棕红色粉末是Fe2O3,灰白色粉末应该含有CaCO3和Fe,为验证自己的判断,美羊羊同学打算进行实验探究,请你一同参与。
标有“成分:CaO、Fe;作用:防潮、防氧化;警告:禁止食用”等字样,撕开小袋,发现里面的固体粉末有少许是棕红色,大多数是灰白色的。经过分析,她认为棕红色粉末是Fe2O3,灰白色粉末应该含有CaCO3和Fe,为验证自己的判断,美羊羊同学打算进行实验探究,请你一同参与。
【实验目的】证实灰白色粉末中含有CaCO3和Fe。
【实验设计】装置如下图所示:
 |
【实验预测与分析】
①若要证实样品中含有CaCO3,观察到的实验现象是 ,B中发生反应的化学方程式为 。
②若要证实样品中含有Fe,E中应该观察到的现象是 ,此时C装置的作用是
③看了美羊羊同学的分析结论,有同学认为小袋内灰白色粉末中还应该有别的物质,![]() 请你写出其中一种物质的化学式 。
请你写出其中一种物质的化学式 。


 甲、乙、丙为初中化学常见物质,甲是石灰石的主要成分,
甲、乙、丙为初中化学常见物质,甲是石灰石的主要成分,
