题目内容
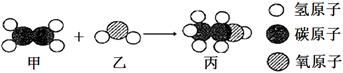
1.6g可燃物在足量的氧气中燃烧,生成4.4g二氧化碳和3.6g水,则关于可燃物的下列判断,正确的是
①可能含有O ②一定不含O ③分子中C、H的原子个数比1︰2
④分子中C、H的原子个数比1︰4
A.①③ B.②④ C.①④ D.②③
B
解析试题分析:在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变;1.6g某物质在氧气中完全燃烧生成4.4g二氧化碳和3.6g水,根据质量守恒定律可知,参加反应的氧气的质量为:4.4g+3.6g-1.6g=6.4g;4.4g二氧化碳中碳元素的质量为:4.4g×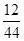 ×100%=1.2g,氧元素的质量为:4.4g-1.2g=3.2g;3.6g水氢元素的质量为:3.6g×
×100%=1.2g,氧元素的质量为:4.4g-1.2g=3.2g;3.6g水氢元素的质量为:3.6g×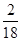 ×100%=0.4g,氧元素的质量为:3.6g-0.4g=3.2g;
×100%=0.4g,氧元素的质量为:3.6g-0.4g=3.2g;
分子中C、H的原子个数比为: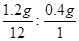 =1:4;由以上计算可知,该物质中含有碳元素和氢元素,不含有氧元素,分子中C、H的原子个数比为1:4.
=1:4;由以上计算可知,该物质中含有碳元素和氢元素,不含有氧元素,分子中C、H的原子个数比为1:4.
考点:质量守恒定律及其应用

取一滤纸条,等间距10滴紫色石蕊试液,然后装入玻璃管中(如图所示),两端管口同时放入分别蘸有浓氨水和浓盐酸的棉球,几秒后观察到图示现象.下列说法不正确的是( )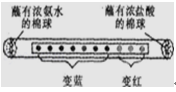
| A.氨水的pH大于7,盐酸的pH小于7 |
| B.浓氨水和浓盐酸都易挥发 |
| C.氨分子和氯化氢分子运动速率都相等 |
| D.酸、碱能使酸碱指示剂显示不同颜色 |
下列有关的化学用语表达正确的是 ( )
| A.五个氢原子:H5 | B.三个水分子:3H2O |
| C.两个钙离子:2Ca+2 | D.四个铵根离子:4NH3+ |
已知 CaO、CuO、SO2、CO2等属于氧化物;NH3、CH4、HF、NaH、KH 等属于氢化物,则下列说法中,错误的是( )
| A.氢化物可理解为由两种元素组成,其中一种是氢元素的化合物 |
| B.水既属于氧化物又属于氢化物 |
| C.氧化物属于含氧化合物 |
| D.在NaH 中,钠元素和氢元素都显+1价 |
意大利罗马大学的科学家获得极具理论研究意义的N4分子,其结构如图所示。下列有关N4的说法正确的是( )
| A.由于N4和N2的分子构成不相同,所以他们的性质不同。 |
| B.N4属于一种新型的化合物 |
| C.N4约占空气体积的78% |
| D.N4是一种混合物 |
镁有“国防金属”的美誉。在元素周期表中,镁元素的信息如图所示,对图中信息解释正确的是 
| A.镁属于非金属元素 | B.镁原子的相对原子质量是24.31g |
| C.镁原子核外电子数是12 | D.镁原子在化学反应中易形成Mg2- |
五氧化二钒(V2O5)是一种催化剂,其中钒元素的化合价为
| A.-2 | B.﹢1 | C.﹢3 | D.﹢5 |