题目内容
13.通过半学期的化学学习,你已经掌握了实验室制取气体的一些规律,以下是老师提供的一些实验装置,根据如图回答问题: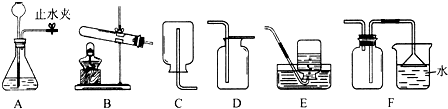
(1)关闭A装置中的止水夹后,从长颈漏斗向锥形瓶中注入一定量的水,表示A装置气密性静置,长颈漏斗中的液面不再下降.
(2)若用B、D装置制取氧气,其反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.检验D中氧气是否收集满的方法是把带火星的木条放到集气瓶口,木条复燃证明已满.
(3)若用B、E装置制取氧气,当集气瓶口出现大气泡后,接下来的操作是用玻璃片盖好集气瓶口后,将集气瓶移出水槽;结束实验时,甲同学先熄灭了酒精灯,忘记将导管从水中取出,在水进入试管之前,可采取的补救措施有:①重新加热至导管口有气泡冒出;②从试管口拔掉带导管的胶塞.
(4)氨气是一种密度比空气小且极易溶于水的气体,有刺激性气味,人吸入能引起呼吸道水肿.当你选用加热氯化铵和氢氧化钙的固体化合物来制取氨气时,你认为收集氨气的装置最好应选择F(填字母),原因是防止氨气污染空气.
分析 表示A装置气密性良好的操作是:关闭A装置中的止水夹后,从长颈漏斗向锥形瓶中注入一定量的水,静置,长颈漏斗中的液面不再下降;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.用玻璃片盖好集气瓶口后,将集气瓶移出水槽,灭了酒精灯,忘记将导管从水中取出,在水进入试管之前,可采取的补救措施有:可采取的补救措施有:①重新加热至导管口有气泡冒出,再移出导管;从试管口拔掉带导管的胶塞.用加热氯化铵和氢氧化钙的固体化合物来制取氨气时,因此需要加热;氨气是一种密度比空气小且极易溶于水的气体,因此收集氨气最好用F,可以防止氨气污染空气.
解答 解:(1)表示A装置气密性良好的操作是:关闭A装置中的止水夹后,从长颈漏斗向锥形瓶中注入一定量的水,静置,长颈漏斗中的液面不再下降;故答案为:静置,长颈漏斗中的液面不再下降(或静置,长颈漏斗中和锥形瓶中的液面差保持不变);
(2)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;把带火星的木条放到集气瓶口,木条复燃证明已满.
(3)若用B、E装置制取氧气,当集气瓶口出现大气泡后,接下来的操作是用玻璃片盖好集气瓶口后,将集气瓶移出水槽;结束实验时,甲同学先熄灭了酒精灯,忘记将导管从水中取出,在水进入试管之前,可采取的补救措施有:重新加热至导管口有气泡冒;从试管口拔掉带导管的胶塞等;故答案为:用玻璃片盖好集气瓶口后,将集气瓶移出水槽;①重新加热至导管口有气泡冒出,再移出导管;②从试管口拔掉带导管的胶塞;
(4)用加热氯化铵和氢氧化钙的固体化合物来制取氨气时,因此需要加热;氨气是一种密度比空气小且极易溶于水的气体,因此收集氨气最好用F,可以防止氨气污染空气;故答案为:F;防止氨气污染空气.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、注意事项、气体的验满方法等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 溶液质量增加 | B. | 溶液温度升高 | ||
| C. | 产生能使澄清石灰水变浑浊的气体 | D. | 固体消失 |
| A. | 除去CO2中CO:通过灼热的氧化铜 | B. | 除去CO中CO2:通入澄清石灰水 | ||
| C. | 除去铜粉中铁粉:加入足量稀盐酸 | D. | 除去铜中氧化铜:加入过量的碳粉 |
| A. | 5.6% | B. | 7.4% | C. | lO% | D. | 小于1% |