题目内容
【题目】A~I为九年级化学所学的物质,已知A为金属氧化物,C为大理石的主要成分,D为蓝色沉淀,E为单质,F为浅绿色溶液,G溶液中的溶质只含两种元素。“→”表示物质间存在着相互转化的关系(部分生成物未标出),如图所示。请回答下列问题:
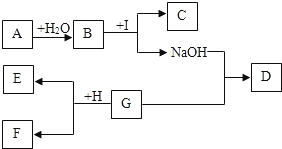
(1)A的化学式是_____。
(2)B与I之间的化学反应属于_______反应(填基本反应类型)
(3)写出G与H反应的化学方程式:________。
【答案】CaO 复分解 Fe + CuCl2=Cu+FeCl2
【解析】
A-I为九年级化学所学的物质,C为大理石的主要成分,所以C是碳酸钙,D为蓝色沉淀, D可能是氢氧化铜沉淀,氢氧化钠与G反应生成氢氧化铜, G溶液中的溶质只含两种元素,氯化铜中含两种元素,氢氧化钠与氯化铜反应生成氢氧化铜和氯化钠,G为氯化铜; E为单质,F为浅绿色溶液,铁和氯化铜反应生成氯化亚铁和铜,H是铁,E是铜;A为金属氧化物,A和水反应生成B,B会与I反应生成碳酸钙沉淀和氢氧化钠,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氧化钙与水反应生成氢氧化钙,A是氧化钙, B是氢氧化钙,I是碳酸钠,经过验证,推导正确。
根据以上分析可知:
(1)A是氧化钙,化学式是CaO;
(2)B与I之间的化学反应是碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,该反应是由两种化合物互相交换成分,生成另外两种化合物的反应,属于复分解反应;
(3)G与H反应是铁和氯化铜反应生成氯化亚铁和铜,反应的化学方程式为:Fe + CuCl2=Cu+FeCl2。

 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
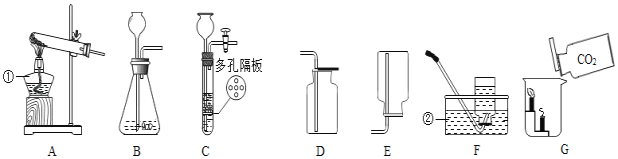
天天向上课时同步训练系列答案【题目】某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,如图,设计实验进行探究。

(提出问题):久置固体的成分是什么?
(查阅资料):铁与氯化铁溶液在常温下发生反应:Fe+2FeCl3=3FeCl2
已知:Ca(OH)2 + Na2CO3=CaCO3↓+2NaOH
打开固体包装观察:部分固体呈黑色,部分固体呈白色,另有少量红棕色的固体。
(作出猜想):久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。
其中可能含有Fe2O3的理由是________________________________。
(实验探究):甲同学的方案:
实验操作 | 实验现象 | 实验结论 |
(1)取少量久置固体于试管中,滴加足量的蒸馏水,搅拌 | 固体溶解,试管外壁发烫 | 固体中一定含有_________ |
(2)过滤,在滤液中滴酚酞溶液 | 溶液变红色 | 固体中一定含有氢氧化钙 |
(3)取滤渣放入试管中,滴加足量的稀盐酸 | 固体逐渐消失,有无色气体产生,得到浅绿色溶液 | 固体中一定有________,一定不含氧化铁 |
(实验质疑):乙同学认为甲同学在实验中得出 “一定不含氧化铁”的结论是错误的,理由是_____________。乙同学认为甲同学实验中一定含有氢氧化钙的结论也不合理,理由是_______________(用化学方程式表示)。
(继续探究)乙同学另取久置的固体进行实验探究:
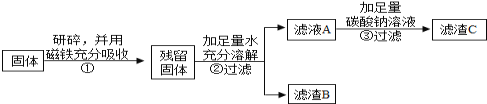
乙同学对滤渣B进行探究:
实验操作 | 实验现象 | 实验结论 |
取滤渣B于试管中,滴加足量的稀盐酸,将气体通入石灰水中。 | 固体逐渐消失,有气泡冒出,石灰水变浑浊,溶液变____________ | 固体中一定含有CaCO3和Fe2O3。写出Fe2O3和稀盐酸反应的化学方程式: _________________________________ |
(综合甲乙同学得出结论):得出久置固体的成分一定有的是__________________________