题目内容
 (1)如图是钙元素在元素周期表中的相关信息及钙原子结构示意图,请根据图示回答问题:
(1)如图是钙元素在元素周期表中的相关信息及钙原子结构示意图,请根据图示回答问题:①钙元素的相对原子质量是
②钙原子在化学反应中易
③钙原子的结构示意图中,m的数值是
(2)实验室用氯化钠固体和水配制5%的氯化钠溶液,步骤为计算、
考点:元素周期表的特点及其应用,一定溶质质量分数的溶液的配制,原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律,溶液、浊液与溶解度
分析:(1)如图是钙元素在元素周期表中的相关信息及钙原子结构示意图,则可知:钙元素的相对原子质量、得失电子情况、根据“原子序数=核内质子数=核外电子数=核电荷数”,可求m的数值.
(2)根据溶液配制的操作步骤分析即可;根据溶解操作所用到的仪器分析即可;根据氯化钠溶液有损失对得到的氯化钠溶液的溶质质量分数不影响进行解答.
(2)根据溶液配制的操作步骤分析即可;根据溶解操作所用到的仪器分析即可;根据氯化钠溶液有损失对得到的氯化钠溶液的溶质质量分数不影响进行解答.
解答:解:(1)①由钙元素在元素周期表中的相关信息,可知钙元素的相对原子质量是40.08;
②由钙元素的原子结构示意图,则可知:最外层电子数为2,钙原子在化学反应中易失电子;
③根据“原子序数=核内质子数=核外电子数=核电荷数”,故钙原子的结构示意图中,m的数值是2+8+8+2=20;
(2)实验室用氯化钠固体和水配制5%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解.溶解时所用的容器是烧杯;若溶解时所用容器内已有少量水,其他操作均规范,则所得溶液中氯化钠的质量不变,溶剂的质量变大,则所得溶液中氯化钠的质量分数偏小.
答案:(1)①40.08; ②失;③20; (2)称量; 烧杯;<.
②由钙元素的原子结构示意图,则可知:最外层电子数为2,钙原子在化学反应中易失电子;
③根据“原子序数=核内质子数=核外电子数=核电荷数”,故钙原子的结构示意图中,m的数值是2+8+8+2=20;
(2)实验室用氯化钠固体和水配制5%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解.溶解时所用的容器是烧杯;若溶解时所用容器内已有少量水,其他操作均规范,则所得溶液中氯化钠的质量不变,溶剂的质量变大,则所得溶液中氯化钠的质量分数偏小.
答案:(1)①40.08; ②失;③20; (2)称量; 烧杯;<.
点评:了解元素周期表的特点及其应用;核外电子在化学反应中的作用;了解原子结构示意图与离子结构示意图的特点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
不能用来鉴别O2和CO2两种气体的是( )
| A、通入澄清石灰水 |
| B、通入紫色石蕊溶液中 |
| C、插入燃着的木条 |
| D、仔细观察颜色 |
澳大利亚科学家发现了纯碳新材料“碳纳米泡沫”,每个泡沫含有约4 000个碳原子,直径约6到9nm,在低于-183℃时,泡沫具有永久磁性.下列叙述正确的是( )
| A、“碳纳米泡沫”是碳单质 |
| B、“碳纳米泡沫”是混合物 |
| C、“碳纳米泡沫”是一种新型的碳化合物 |
| D、“碳纳米泡沫”和金刚石的物理性质完全相同 |
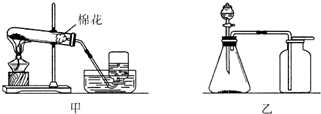 如图是实验室制取氧气的两种装置,请回答下列问题.
如图是实验室制取氧气的两种装置,请回答下列问题.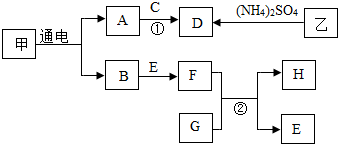 如图所示的集中常见物质转化关系.A~H及甲、乙分别表示不同物质,其中A、B、C、H均为无色无味气体,D为刺激性气味气体,E为生产、生活中应用量最大的金属单质,乙可用于中和土壤酸性;反应①为化合反应.(部分反应物、生成物及反应条件已略去).请回答下列问题:
如图所示的集中常见物质转化关系.A~H及甲、乙分别表示不同物质,其中A、B、C、H均为无色无味气体,D为刺激性气味气体,E为生产、生活中应用量最大的金属单质,乙可用于中和土壤酸性;反应①为化合反应.(部分反应物、生成物及反应条件已略去).请回答下列问题: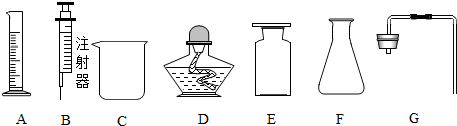
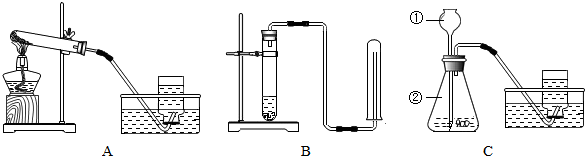
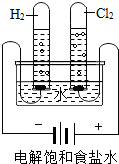 工业上通过电解饱和食盐水制取烧碱、氯气和氢气,称为氯碱工业.如图是实验室电解饱和食盐水的实验结果.
工业上通过电解饱和食盐水制取烧碱、氯气和氢气,称为氯碱工业.如图是实验室电解饱和食盐水的实验结果.