题目内容
【题目】利用海水淡化后母液中含有的氯化镁和海边盛产的贝壳主要成分,制取金属镁,生产大致流程如图所示:
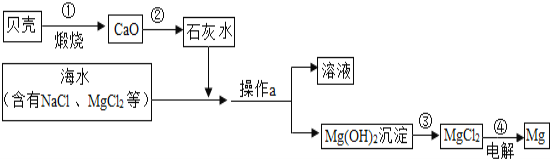
(1)请写出母液中氯化镁转化为氢氧化镁的化学方程式:________
(2)操作a的名称是 ______,步骤 ③加入的物质是_____
(3)工业上常以氯化镁为原料,电解就可以生产金属镁反应的化学方程式为___
(4)海水制镁过程中没涉及到的反应类型是___________
【答案】MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓ 过滤 稀盐酸 MgCl2![]() Mg+Cl2↑ 置换反应
Mg+Cl2↑ 置换反应
【解析】
(1)由反应的流程可知,氯化镁转化为氢氧化镁的反应是氯化镁与氢氧化钙反应生成了氢氧化镁沉淀和氯化钙,反应的化学方程式是:MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓;
(2)由反应的流程可知,操作a是将固体和液体分开,操作的名称是过滤;步骤③是将Mg(OH)2转化MgCl2,氢氧化镁与盐酸反应生成氯化镁和水,所以加入的物质是稀盐酸;
(3)由反应的流程可知,电解氯化镁生成了镁,根据质量守恒定律可知,另一种产生是氯气,化学方程式为:MgCl2![]() Mg+Cl2↑;
Mg+Cl2↑;
(4)反应①是碳酸钙煅烧生成氧化钙和二氧化碳,该反应是由一种物质生成两种物质的反应,属于分解反应;反应②是氧化钙与水反应生成氢氧化钙,该反应是由两种物质生成一种物质的反应,属于化合反应;反应③是氢氧化镁与盐酸反应生成氯化镁和水,该反应是由两种化合物互相交换成分,生成另外两种化合物的反应,属于复分解反应;反应④是电解氯化镁生成镁和氯气,该反应是由一种物质生成两种物质的反应,属于分解反应。海水制镁过程中没涉及到的反应类型是置换反应。

 阅读快车系列答案
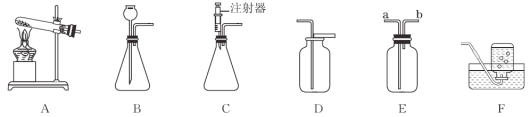
阅读快车系列答案【题目】根据下图所示实验分析得出的结论中,不正确的是
|
|
|
|
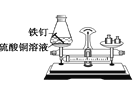
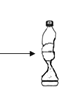
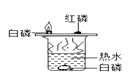
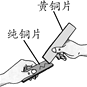
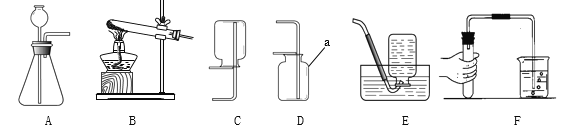
A.可以验证质量守恒定律 | B.常温下,二氧化碳能溶于水 | C.只能探究可燃物的燃烧需要的一个条件 | D.黄铜的硬度比纯铜的大 |
A. A B. B C. C D. D