题目内容
【题目】工业上以黄铁矿(主要成分是FeS2)为原料生产硫酸,请结合生产硫酸的简要流程图完成下面的问题: 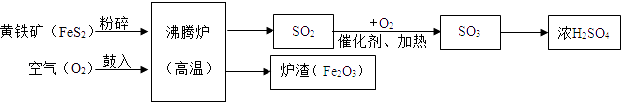
(1)写出流程图中一种氧化物的名称;
(2)将黄铁矿粉碎,目的是;
(3)流程中SO3转化为H2SO4的化学方程式为;
(4)实验室稀释浓硫酸的正确操作方法是 .
【答案】
(1)二氧化硫或三氧化硫或三氧化二铁
(2)增大反应物的接触面积
(3)SO3+H2O=H2SO4
(4)将浓硫酸沿器壁慢慢倒入水中,边倒边搅拌,且不可将水倒入浓硫酸中
【解析】解:(1)二氧化硫或三氧化硫或三氧化二铁都是由两种元素组成,一种元素是氧元素,属于氧化物;(2)反应物接触面积越大,反应越剧烈,黄铁矿粉碎会增大反应物的接触面积,加快反应速度;(3)流程中SO3转化为H2SO4的反应是三氧化硫和水反应生成硫酸,反应的化学方程式为:SO3+H2O=H2SO4;(4)浓硫酸的稀释方法是:将浓硫酸沿着容器壁慢慢倒入水中,并用玻璃棒不断搅拌. 所以答案是:(1)二氧化硫或三氧化硫或三氧化二铁.(2)增大反应物的接触面积.(3)SO3+H2O=H2SO4 . (4)将浓硫酸沿器壁慢慢倒入水中,边倒边搅拌,且不可将水倒入浓硫酸中.
【考点精析】本题主要考查了书写化学方程式、文字表达式、电离方程式和从组成上识别氧化物的相关知识点,需要掌握注意:a、配平 b、条件 c、箭号;氧化物必须是由两种元素组成,而且是化合物.如:H2O、AI2O3、HCI 都是氧化物,它们也属于化合物,又是纯净物才能正确解答此题.

练习册系列答案
相关题目