题目内容
实验室用石灰石与稀盐酸反应制取二氧化碳.若要制取4.4 g二氧化碳,需要溶质的质量分数为10%的盐酸多少克?
解:设所用盐酸中溶质的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
x 4.4g
 =
=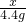 ,x=7.3g
,x=7.3g
所用盐酸的质量为7.3g÷10%=73g
答:需要溶质的质量分数为10%的盐酸73g.
分析:由二氧化碳的质量根据碳酸钙与盐酸反应的化学方程式可以计算出所用盐酸中溶质的质量,再根据溶质质量分数的计算公式结合盐酸的溶质质量分数就能计算出盐酸的质量.
点评:本题主要考查有关化学方程式的计算和溶质质量分数的计算,难度稍大.
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
x 4.4g
 =
=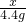 ,x=7.3g
,x=7.3g所用盐酸的质量为7.3g÷10%=73g
答:需要溶质的质量分数为10%的盐酸73g.
分析:由二氧化碳的质量根据碳酸钙与盐酸反应的化学方程式可以计算出所用盐酸中溶质的质量,再根据溶质质量分数的计算公式结合盐酸的溶质质量分数就能计算出盐酸的质量.
点评:本题主要考查有关化学方程式的计算和溶质质量分数的计算,难度稍大.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
酸、碱、盐溶解性表是学习化学的重要工具.下表列出了“部分酸、碱、盐在20℃时的溶解性”.试一试你能利用此表完成以下任务:
| OH- | NO3- | Cl- | CO32- | SO42- | |
| H+ | -- | 溶、挥 | 溶、挥 | 溶、挥 | 溶 |
| Na- | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 溶 | 不 | 微 |
| Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
(2)实验室制取二氧化碳用石灰石和稀盐酸反应,一般不用稀硫酸的原因是什么?
酸、碱、盐溶解性表是学习化学的重要工具.下表列出了“部分酸、碱、盐在20℃时的溶解性”.试一试你能利用此表完成以下任务:
(1)说出碳酸溶液与硝酸钡溶液能发出反应的理由.
(2)实验室制取二氧化碳用石灰石和稀盐酸反应,一般不用稀硫酸的原因是什么?
| OH- | NO3- | Cl- | CO32- | SO42- | |
| H+ | -- | 溶、挥 | 溶、挥 | 溶、挥 | 溶 |
| Na- | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 溶 | 不 | 微 |
| Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
(2)实验室制取二氧化碳用石灰石和稀盐酸反应,一般不用稀硫酸的原因是什么?