题目内容
【题目】化学是以实验为基础的科学,实验是科学探究的重要手段。
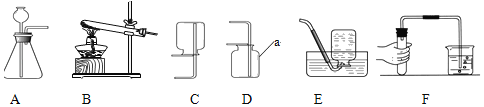
(1)酸和碱之间发生中和反应。如下图所示的三个实验均可验证酸与碱能发生反应。
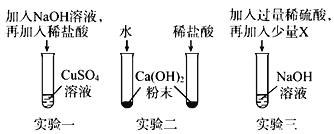
①实验一中,通过稀盐酸与________(填写化学式)反应的现象,验证了酸与碱发生了反应。
②实验二通过两支试管中的现象对比,可以判断稀盐酸与Ca(OH)2能反应,该实验除需控制所加水和稀盐酸的温度、体积相同外,还需控制____________相同。
③实验三中,若加入X可验证稀硫酸与碱能发生反应,则符合此条件的X是下列物质中的_____(填字母即可)。
a 无色酚酞溶液 b 铁粉 c 氧化铜 d 碳酸钠
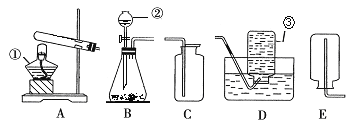
(2)为了探究二氧化碳与氢氧化钠发生反应,河南省实验中学化学兴趣小组进行了如甲所示实验;并利用了数字化实验手段进行了探究:在用排空气法收集到的二氧化碳集气瓶内加入足量氢氧化钠溶液,通过压强传感器和数据采集器得到的图象如乙所示。

①实验甲装置A中发生反应的化学方程式为__________________________;
②甲所示装置B中的实验现象是什么________?
③乙中图示曲线总体趋势为数据逐渐减小,其中的道理是什么________?
(3)向盛有20g氢氧化钠溶液的烧杯中加入20mL质量分数为7.3%的稀盐酸,恰好完全反应。则所用氢氧化钠溶液中溶质的质量分数是多少________? (提示:7.3%的稀盐酸密度约为1.035g/mL)
【答案】Cu(OH)2 氢氧化钙粉末的质量 a CaCO3+2HCl═CaCl2+H2O+CO2↑ 有白色沉淀生成 二氧化碳与氢氧化钠反应,装置内气压减小 8.28%
【解析】
(1)①实验一中,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀,加入盐酸后,沉淀消失,溶液变蓝,通过稀盐酸与Cu(OH)2反应的现象,验证了酸与碱发生了反应;
②实验二通过对比两支试管中温度变化,可以判断稀盐酸与Ca(OH)2能反应,该实验除需控制所加水和稀盐酸的温度、体积相同外,还需控制氢氧化钙粉末的质量相同;
③由图可知,实验三中先加入过量硫酸,然后加入的X,如果X本身能与碱反应,且有现象,但加入后却没看到相应现象,则证明氢氧化钠已经被硫酸反应掉,则可证明中和反应发生了。无色酚酞溶液,不变红,说明氢氧化钠被硫酸反应;铁粉、氧化铜、碳酸钠不与氢氧化钠不反应,无法证明。故选a;
(2)①实验甲装置A中发生反应是碳酸钙和稀盐酸反应生成二氧化碳、氯化钙、水,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
②二氧化碳和氢氧化钠反应生成碳酸钠,碳酸钠和硝酸钡反应生成碳酸钡沉淀,甲所示装置B中的实验现象是生成白色沉淀;
③乙中图示曲线总体趋势为数据逐渐减小,其中的道理是二氧化碳与氢氧化钠反应,装置内气体减少,导致气压减小;
(3)20mL质量分数为7.3%的稀盐酸中氯化氢的质量为:20mL×1.035g/mL×7.3%=20.7g×7.3%;
设20g氢氧化钠溶液中氢氧化钠的质量为x
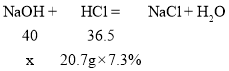
![]()
x=1.656g
氢氧化钠溶液中溶质的质量分数是1.656g÷20g×100%=8.28%。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案【题目】化学实验常用二氧化锰催化过氧化氢分解制取氧气。针对影响过氧化氢分解速率速率的因素有哪些?某化学兴趣小组对此进行以下探究;
序号 | 过氧化氢溶液的浓度/% | 过氧化氢溶液的质量/g | 温度/℃ | 二氧化锰的质量/g | 氧气的体积/mL | 时间/s |
① | 5 | 12 | 20 | 0.2g | 125 | 20 |
② | 30 | 12 | 20 | 0.2g | 125 | 2 |
③ | 3 | 12 | 40 | ﹣ | 125 | 148 |
(提出问题)影响过氧化氢分解速率因素有哪些?
(猜想与假设)假设1:过氧化氢的浓度;假设2:催化剂的质量;
假设3:实验的温度;假设4:_____(请你提出一种假设)
(设计实验方案)小明设计如下实验进行验证。
(1)通过对比实验①和②可知,过氧化氢分解的速率与_____有关。
(2)二氧化锰在过氧化氢分解前后质量和_____不变。
(讨论交流)(3)小燕认为在这个实验中,必须使用排水法收集氧气,理由是:_____
(3)小辉认为小明的方案无法验证温度对过氧化氢分解速率的影响。请你帮他说出理由:_____
(拓展延伸)同学们查阅资料后得知,氯化铁溶液对过氧化氢分解也有影响。因此设计实验继续探究。向2支试管中分别加入等质量不同浓度的过氧化氢溶液,再加入等质量、等浓度的氯化铁溶液,分别用气压传感器测定两支试管中气压的变化曲线。如图下:
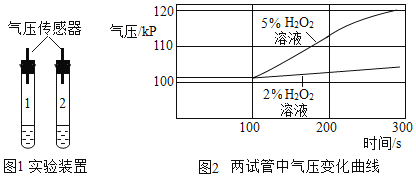
(5)为确保实验准确性,请你设计向两试管中加入氯化铁溶液的具体方法:_____
(6)请你从曲线中总结出氯化铁溶液对过氧化氢分解影响的两点规律性结论:_____
【题目】2019年是化学元素周期表国际年。下边表格是元素周期表一部分。这些元素均位于第_____周期;铝原子结构示意图为______;现有相等质量的这几种金属元素,则其所含原子个数由多到少的顺序是____________。
11 Na 23.00 | 12 Mg 24.31 | 13 Al 26.98 | 14 Si 28.09 |