题目内容
(2005?怀化)某同学做证明鸡蛋壳的主要成分是碳酸盐的实验时,设计了如下方案(如图所示),经检验装置气密性合格后加入试剂
结果发现B中变浑浊
(1)描述A中出现的现象
(2)分析C和D中可能出现的现象:C中
(3)写出B中反应的化学方程式
(4)根据所学知识,你认为上述方案中:
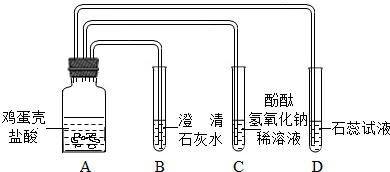
结果发现B中变浑浊
(1)描述A中出现的现象
鸡蛋壳逐渐溶解,有大量气泡产生
鸡蛋壳逐渐溶解,有大量气泡产生
(2)分析C和D中可能出现的现象:C中
红色逐渐变浅,最后完全消失(或红色逐渐变成无色)
红色逐渐变浅,最后完全消失(或红色逐渐变成无色)
,D中溶液由紫色变成红色
溶液由紫色变成红色
(3)写出B中反应的化学方程式
CO2+Ca(OH)2═CaCO3↓+H2O
CO2+Ca(OH)2═CaCO3↓+H2O
(4)根据所学知识,你认为上述方案中:
AB
AB
(填图中序号)组合一起足以证明鸡蛋壳的主要成分是碳酸盐.
分析:本题要证明的是碳酸盐,碳酸盐的检验方法是:加入稀盐酸,如果生成气体,把生成的气体通入澄清石灰水中,看是否变浑浊,如果变浑浊,则说明是碳酸盐,反之不是;二氧化碳的水溶液显酸性,不能是酚酞试液变色,可以使紫色的石蕊试液变成红色.
解答:解:(1)把鸡蛋壳加入盐酸中,鸡蛋壳会和盐酸反应生成气体二氧化碳;故本题答案为:鸡蛋壳逐渐溶解,产生大量气泡;
(2)因为CO2可以与氢氧化钠反应,同时也可以使紫色石蕊试液变红,故本题答案为:C中红色逐渐变浅,最后完全消失(或红色逐渐变成无色),D中溶液由紫色变成红色;
(3)二氧化碳可以和氢氧化钙反应产生碳酸钙沉淀和水,反应的方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;故本题答案为:CO2+Ca(OH)2═CaCO3↓+H2O;
(4)根据所学知识及实验,通过前两步即可确认鸡蛋壳中含有碳酸盐:能够和酸反应产生气泡,且该气体能够使澄清的石灰水变浑浊,所以没有必要再做C和D的实验了,故本题答案为:AB.
(2)因为CO2可以与氢氧化钠反应,同时也可以使紫色石蕊试液变红,故本题答案为:C中红色逐渐变浅,最后完全消失(或红色逐渐变成无色),D中溶液由紫色变成红色;
(3)二氧化碳可以和氢氧化钙反应产生碳酸钙沉淀和水,反应的方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;故本题答案为:CO2+Ca(OH)2═CaCO3↓+H2O;
(4)根据所学知识及实验,通过前两步即可确认鸡蛋壳中含有碳酸盐:能够和酸反应产生气泡,且该气体能够使澄清的石灰水变浑浊,所以没有必要再做C和D的实验了,故本题答案为:AB.
点评:本题是离子的鉴别题,关键是抓住本离子与其他离子的性质不同之处,石灰石、大理石、鸡蛋壳的主要成分都是碳酸钙,都含有碳酸根,和酸反应能生成二氧化碳,检验二氧化碳的生成只能用澄清石灰水,不能用紫色石蕊试液.

练习册系列答案
相关题目