题目内容
现有一包白色固体混合物,可能由BaCl2、KNO3、CuSO4、FeCl3、Na2CO3、Na2SO4、NaCl中的几种混合而成,为了证明其组成,作如下实验:
(1)取一定量该固体混合物加入足量的水,充分搅拌,得到白色沉淀和无色溶液。过滤得到白色沉淀A,无色滤液B;
(2)向白色沉淀A中加入过量的盐酸溶液,沉淀部分溶解;
(3)向无色滤液B中加入硝酸银溶液,产生不溶于稀硝酸的白色沉淀。下列说法正确的是________
(1)取一定量该固体混合物加入足量的水,充分搅拌,得到白色沉淀和无色溶液。过滤得到白色沉淀A,无色滤液B;
(2)向白色沉淀A中加入过量的盐酸溶液,沉淀部分溶解;
(3)向无色滤液B中加入硝酸银溶液,产生不溶于稀硝酸的白色沉淀。下列说法正确的是________
| A.固体混合物中一定含有BaCl2、FeCl3、Na2CO3、Na2SO4,可能含有NaCl |
| B.固体混合物中一定含有BaCl2、Na2CO3、Na2SO4,可能含有NaCl、KNO3 |
| C.固体混合物中一定含有BaCl2、、CuSO4、 NaCl,一定不含有FeCl3、Na2CO3、KNO3 |
| D.固体混合物中一定含有BaCl2、Na2SO4、NaCl,一定不含有FeCl3、CuSO4 |
B
试题分析:通过步骤(1)可知,原白色固体混合物中一定不含有CuSO4和FeCl3,因为它们的水溶液是有颜色的,通过步骤(2)可知,沉淀中一定同时含有BaSO4和BaCO3,因为BaSO4不能与稀盐酸反应,BaCO3能与稀盐酸反应,由此可以确定原白色固体中一定含有BaCl2、Na2CO3、Na2SO4;通过步骤(3)可知,原白色固体中一定含有氯元素,根据以上信息可知原白色固体中一定含有BaCl2、Na2CO3、Na2SO4,是否含有NaCl、KNO3没法确定,一定不会含有CuSO4和FeCl3。

练习册系列答案
相关题目
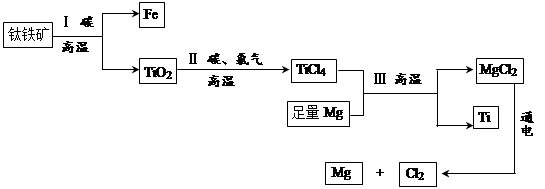
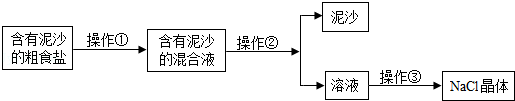
 ),则可能的原因是(填字母) .
),则可能的原因是(填字母) .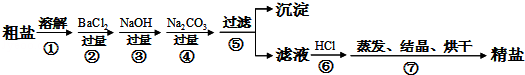

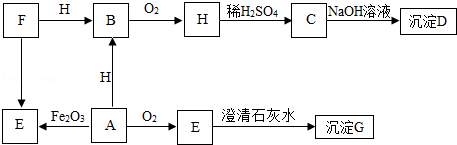
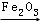 E化学方程式
E化学方程式