题目内容
【题目】一定条件下,在密闭容器内投入甲、乙、丙、丁四种物质,在不同时刻测得容器内各物质的质量如下表所示,下列说法不正确的是
物质 时刻 | 甲 | 乙 | 丙 | 丁 |
起始 | 80g | 5g | 100g | 5g |
t1 | a | 55g | 60g | 5g |
t2 | b | c | 40g | 5g |
A.甲是反应物,乙是生成物B.丁可能是该反应的催化剂
C.a = 70g,c = 80gD.该反应可能是N2+3H2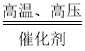 2NH3
2NH3
【答案】D
【解析】
A、根据质量守恒定律,化学反应前后,物质的总质量不变,故80g+5g+100g+5g=a+55g+60g+5g,a=70g,反应后,甲的质量减少,甲是反应物,乙的质量增加,乙是生成物,丙的质量减少,丙是反应物,不符合题意;
B、反应前后,丁的质量不变,丁可能是催化剂,也可能是不参与反应的杂质,不符合题意;
C、反应过程中,乙、丙的质量比为:(c-55g):(60g-40g)=(55g-5g):(100g-60g),c=80g,a=70g,不符合题意;
D、在反应过程中乙、丙的质量比为5:4, 中,三种物质的质量比为:(14×2):6:(17×2)=14:3:17,符合题意。
中,三种物质的质量比为:(14×2):6:(17×2)=14:3:17,符合题意。
故选D。

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目