题目内容
【题目】2017年12月18日,南通地铁正式开建,标志着南通进入“地铁时代”。
(1)地铁列车车体大量使用的镁铝合金属于_____(填“金属材料”或“合成材料”),镁铝合金的优点是_____。
(2)地铁建造过程中需要使用大量的钢铁。工业炼铁可利用一氧化碳与氧化铁反应,写出该反应的化学方程式:_____。
(3)地铁信息传输系统中使用的光导纤维和电子芯片的关键材料分别为二氧化硅(SiO2)和晶体硅(Si)。将二氧化硅转化为硅的过程属于_____(填“物理变化”或“化学变化”)。
(4)地铁施工过程中产生的废水、废浆以及机械漏油等,都会对水体产生污染。使用活性炭可对污水进行处理,这是利用了活性炭的_____性。
(5)为确保消防安全,地铁隧道中须安装自动喷淋系统。喷出的水能灭火的原因是_____。
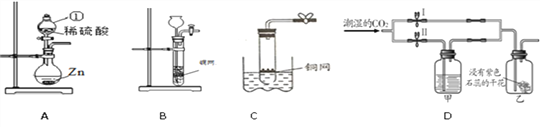
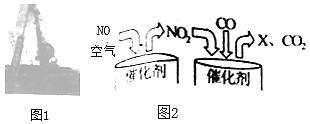
(6)地铁施工工程车的尾气中含NO、CO.尾气经过如图2所示催化转化后,可实现达标排放。写出单质X的化学式:_____。
【答案】 金属材料; 密度小,硬度大,耐腐蚀 3CO+Fe2O3![]() 2Fe+3CO2 化学变化 吸附 水洒在火上后会迅速蒸发,蒸发会带走大量的热使温度减低,当温度达到着火点以下时火就会熄灭 N2
2Fe+3CO2 化学变化 吸附 水洒在火上后会迅速蒸发,蒸发会带走大量的热使温度减低,当温度达到着火点以下时火就会熄灭 N2
【解析】
考查常见的材料以及不同材料的优缺点,化学方程式的书写,物质的变化和性质,灭火的原理和质量守恒定律等。
(1)镁铝合金属于金属材料,镁铝合金具有的优点是密度小,硬度大,耐腐蚀;(2)工业炼铁的原理是一氧化碳和氧化铁在高温的条件下反应生成二氧化碳和铁,反应的化学方程式是3CO+Fe2O3![]() 2Fe+3CO2;(3)二氧化硅和硅是两种不同的物质,有新物种生成的变化属于化学变化;(4)活性炭具有吸附性,可以吸附色素和异味;(5)水蒸发吸热,可以使环境的温度降到可燃物的着火点以下,破坏燃烧的条件,达到灭火的目的;(6)根据质量守恒定律,反应前后元素的种类不会发生改变,所以单质x是由氮元素组成的单质即氮气。
2Fe+3CO2;(3)二氧化硅和硅是两种不同的物质,有新物种生成的变化属于化学变化;(4)活性炭具有吸附性,可以吸附色素和异味;(5)水蒸发吸热,可以使环境的温度降到可燃物的着火点以下,破坏燃烧的条件,达到灭火的目的;(6)根据质量守恒定律,反应前后元素的种类不会发生改变,所以单质x是由氮元素组成的单质即氮气。