题目内容
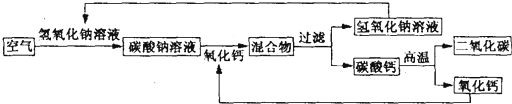
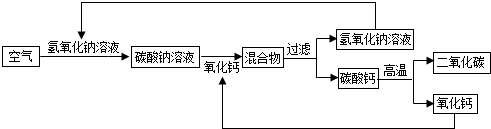
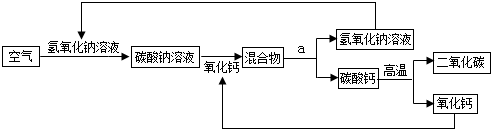
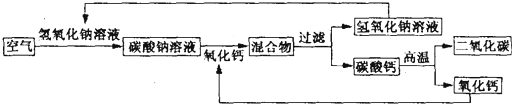
从空气中分离二氧化碳可设计如下的操作方案,其基本流程如图所示(部分条件未标出).
(1)写出流程中生成碳酸钙和氢氧化钠的化学方程式 .
(2)写出流程中涉及到的有关化学方程式:化合反应 ;分解反应 .
(3)整个流程中,除水外,还有二种可以循环利用的物质是 (写化学式).
【答案】分析:(1)依据生成物可推出反应物,然后再写出方程式;
(2)依据反应流程图分析发生的化学反应,并结合反应特点书写方程式,化合反应是‘多合一’,分解反应是‘一分多’;
(3)可循环使用的物质是在前面的反应物中出现过,到了后面的生成物中又出现的物质,据此分析解答.
解答:解:(1)根据生成物是碳酸钙和氢氧化钠,将其相互交换成分就是反应物碳酸钠和氢氧化钙,所以反应物是碳酸钠和氢氧化钙,生成物是碳酸钙和氢氧化钠,用观察法配平即可,所以方程式为:Ca(OH)2+Na2C03=CaC03↓+2NaOH;
(2)根据反应流程图可知:氧化钙和水反应生成氢氧化钙,是由两种物质生成一种物质,属于化合反应,碳酸钙高温分解生成二氧化碳和氧化钙,是由一种物质反应生成两种物质,属于分解反应;
(3)碳酸钠和氢氧化钙反应生成了碳酸钙和氢氧化钠,而在前面空气和氢氧化钠反应生成碳酸钠,所以氢氧化钠可以循环使用;碳酸钙高温生成了氧化钙和二氧化碳,在前面氧化钙与碳酸钠溶液反应,所以氧化钙也可以循环使用;
故答案为:(1)Ca(OH)2+Na2CO3═2NaOH+CaCO3↓;
(2)CaO+H2O═Ca(OH)2; CaCO3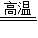 CaO+CO2↑;
CaO+CO2↑;
(3)NaOH、CaO.
点评:解答本题的关键是能据流程图分析发生的化学反应,明确可循环使用物质的找法:是前面反应物中出现,后面的生成物中出现的物质.
(2)依据反应流程图分析发生的化学反应,并结合反应特点书写方程式,化合反应是‘多合一’,分解反应是‘一分多’;
(3)可循环使用的物质是在前面的反应物中出现过,到了后面的生成物中又出现的物质,据此分析解答.
解答:解:(1)根据生成物是碳酸钙和氢氧化钠,将其相互交换成分就是反应物碳酸钠和氢氧化钙,所以反应物是碳酸钠和氢氧化钙,生成物是碳酸钙和氢氧化钠,用观察法配平即可,所以方程式为:Ca(OH)2+Na2C03=CaC03↓+2NaOH;
(2)根据反应流程图可知:氧化钙和水反应生成氢氧化钙,是由两种物质生成一种物质,属于化合反应,碳酸钙高温分解生成二氧化碳和氧化钙,是由一种物质反应生成两种物质,属于分解反应;
(3)碳酸钠和氢氧化钙反应生成了碳酸钙和氢氧化钠,而在前面空气和氢氧化钠反应生成碳酸钠,所以氢氧化钠可以循环使用;碳酸钙高温生成了氧化钙和二氧化碳,在前面氧化钙与碳酸钠溶液反应,所以氧化钙也可以循环使用;
故答案为:(1)Ca(OH)2+Na2CO3═2NaOH+CaCO3↓;
(2)CaO+H2O═Ca(OH)2; CaCO3
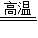 CaO+CO2↑;
CaO+CO2↑;(3)NaOH、CaO.
点评:解答本题的关键是能据流程图分析发生的化学反应,明确可循环使用物质的找法:是前面反应物中出现,后面的生成物中出现的物质.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目