题目内容
 (2012?泰安)小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:①在三个烧杯中分别加入11.0g样品及足量的水配成溶液;②向三个烧杯中分别加入一定质量的10.0%氯化钙溶液;③将充分反应后生成的沉淀过滤、洗涤、干燥,并称量得到的白色固体.
(2012?泰安)小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:①在三个烧杯中分别加入11.0g样品及足量的水配成溶液;②向三个烧杯中分别加入一定质量的10.0%氯化钙溶液;③将充分反应后生成的沉淀过滤、洗涤、干燥,并称量得到的白色固体.实验所得数据见下表,请你分析并进行有关计算:?
| 烧杯Ⅰ | 烧杯Ⅱ | 烧杯Ⅲ | |
| 加入10.0%氯化钙溶液的质量(g) | 55.5 | 120.0 | 150.0 |
| 白色固体的质量(g) | 5.0 | 10.0 | 10.0 |
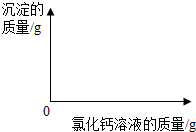
(2)在如图中绘制出白色沉淀与加入氯化钙溶液的质量关系图(图上要注明白色沉淀、氯化钙溶液的相关质量).
分析:(1)分析表格中的数据可以知道11.0g样品最多生成10.0g沉淀,可以据此结合碳酸钠和氯化钙反应的化学方程式进而求算出碳酸钠的质量分数;
(2)根据图表信息可以知道比较烧杯Ⅰ和烧杯Ⅱ中的数据可以知道,55.5g氯化钙溶液可以和碳酸钠反应生成5.0g沉淀,那么产生10.0g沉淀,所需氯化钙溶液的质量为111.0g,可以据此作图即可完成解答.
(2)根据图表信息可以知道比较烧杯Ⅰ和烧杯Ⅱ中的数据可以知道,55.5g氯化钙溶液可以和碳酸钠反应生成5.0g沉淀,那么产生10.0g沉淀,所需氯化钙溶液的质量为111.0g,可以据此作图即可完成解答.
解答:解:?由实验数据可知,11.0g样品中的碳酸钠与氯化钙溶液充分反应最多生成10.0g碳酸钙.
(1)设要生成10.0g碳酸钙需要碳酸钠的质量为X?
Na2CO3+CaCl2═CaCO3↓+2NaCl?
106 100?
x 10.0g
=
?
解得:x=10.6g?
样品中碳酸钠的质量分数为:
×100%=96.4%;
答:样品中碳酸钠的质量分数是96.4%.
(2)?根据图表信息可以知道比较烧杯Ⅰ和烧杯Ⅱ中的数据可以知道,55.5g氯化钙溶液可以和碳酸钠反应生成5.0g沉淀,那么产生10.0g沉淀,所需氯化钙溶液的质量为111.0g,可以据此作图为:

故答案为:(1)96.4%;
(2).
(1)设要生成10.0g碳酸钙需要碳酸钠的质量为X?
Na2CO3+CaCl2═CaCO3↓+2NaCl?
106 100?
x 10.0g
| 106 |
| x |
| 100 |
| 10.0g |
解得:x=10.6g?
样品中碳酸钠的质量分数为:
| 10.6g |
| 11.0g |
答:样品中碳酸钠的质量分数是96.4%.
(2)?根据图表信息可以知道比较烧杯Ⅰ和烧杯Ⅱ中的数据可以知道,55.5g氯化钙溶液可以和碳酸钠反应生成5.0g沉淀,那么产生10.0g沉淀,所需氯化钙溶液的质量为111.0g,可以据此作图为:

故答案为:(1)96.4%;
(2).

点评:解答这类题目时,首先,要熟记和理解有关含杂质物质的化学反应的有关计算的方法、步骤和格式等相关知识;然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,特别是有关化学方程式的书写和意义、不纯物质的质量与纯物质的质量的相互转化方法,以及根据化学方程式计算的方法、步骤和格式等,细致地阅读、分析题意,联系着生产、生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目

